Bioénergétique
Cycle de Krebs (cycle de l'acide citrique)
Bilan et régulation
- Biochimie
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Le cycle de Krebs ou cycle de l'acide citrique mitochondrial produit 4 molécules de coenzymes sous forme réduite, 3 NADH et 1 FADH2, et une molécule de GTP/ATP.
Bilan du cycle de Krebs
1. Le bilan général du cycle de Krebs est le suivant.
$\ce{Acétyl-CoA + 2H2O + 3NAD+ + FAD + GDP/ADP + Pi}$
$\longrightarrow$ $\ce{2CO2 + 3(NADH + H+) + FADH_2 + GTP/ATP + CoA}$
En conclusion, par molécule de pyruvate, nous avons la formation de :
- 2 $\ce{CO2}$,
- 4 molécules de coenzymes sous forme réduite, 3 NADH et 1 FADH2,
- 1 GTP, dans le foie ou 1 ATP, dans les muscles, composés à liaison phosphate riche en énergie, selon les cellules.
2. Le cycle de Krebs ne produit directement qu'un ATP à la différence de la glycolyse qui en forme 2, i.e. les deux autres étant consommés par les phosphorylations des intermédiaires (
3. Cependant, le rendement énergétique réel du cycle est beaucoup plus élevé grâce aux coenzymes réduites générées, i.e. 3 NADH et 1 FADH2, utilisées ensuite par la chaîne respiratoire des mitochondries pour former à leur tour des molécules d’ATP supplémentaires par la phosphorylation oxydative.
- Un NADH fournit environ 2,5 ATP, soit 7,5 ATP,
- 1 FADH2 fournit environ 1,5 ATP.
Le total, en rajoutant l'ATP produit, est donc d'environ 10 ATP.

N'oublions pas que la glycolyse convertit une molécule de glucose en deux molécules de pyruvate, il faut donc multiplier le bilan par deux en partant de ce processus (
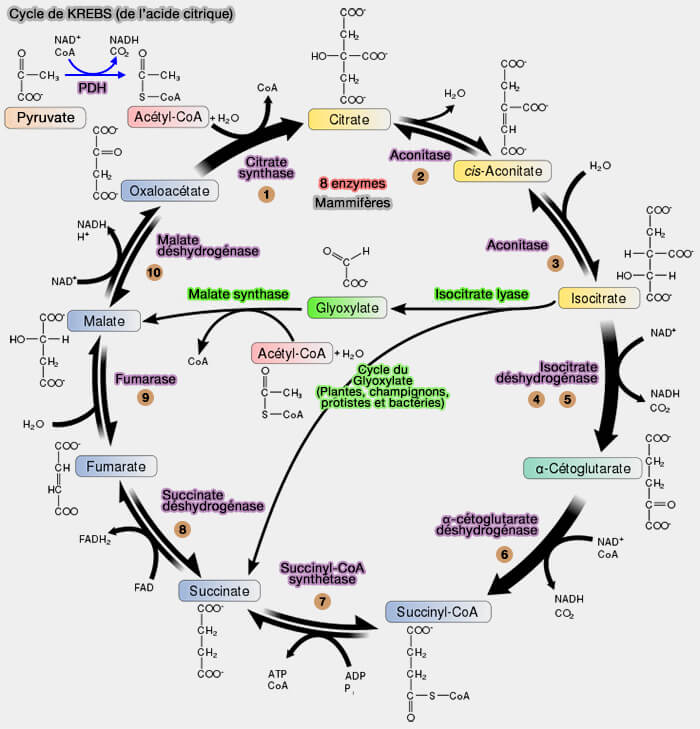
(Figure : vetopsy.fr d'après Agrotman)
Régulation du cycle de Krebs
1. La charge énergétique de la cellule, i.e. rapports ATP/ADP, NADH/NAD+…, joue un rôle prédominant sur l'intensité de fonctionnement du cycle de Krebs.
a. Ces rapports influencent directement l’activité des enzymes clés du cycle, mais aussi indirectement via l’activation de capteurs énergétiques comme :
- AMPK (AMP-activated protein kinase),
- mTOR (mammalian Target Of Rapamycin),
- les sirtuines.
b. Ces capteurs permettent une intégration fine du statut énergétique pour ajuster l’activité métabolique, y compris celle du cycle de Krebs, en fonction des besoins cellulaires.

La charge énergétique cellulaire est étudiée dans un chapitre spécifique.
1. L'entrée du pyruvate dans le cycle de Krebs, via sa conversion en acétyl-CoA, par le complexe pyruvate déshydrogénase (PDH), est freinée lorsque de l'élévation de la concentration :
- en NADH, i.e. signal d’un état énergétique suffisant,
- en acétyl-CoA, i.e. rétro-inhibition, signalant une surcharge du cycle.
Ces deux métabolites agissent comme des inhibiteurs allostériques du complexe pyruvate déshydrogénase (PDH), i.e. ils se lient à des sites spécifiques du complexe, différents du site actif, provoquant un changement de conformation qui diminue son activité.
2. De même, un excès d'ATP, reflet d’une haute charge énergétique, tend à inhiber la pyruvate déshydrogénase (PDH), par trois mécanismes :
- inhibition allostérique directe,
- phosphorylation de la PDH par la pyruvate déshydrogénase kinase (PDK),
- effet indirect sur les rapports ATP/ADP et NADH/NAD+, i.e. des niveaux élevés d’ATP s’accompagnent généralement d’une augmentation du NADH et de l’acétyl-CoA, renforçant ainsi l’inhibition du PDH.
3. Par contre, une augmentation de la concentration en AMP, produit par l'hydrolyse de l'ATP et l'ADP, signalant que la cellule est en situation de faible énergie disponible,
L’AMP agit comme un activateur de plusieurs enzymes et voies métaboliques qui augmentent la production d’ATP comme (
- activation de la glycolyse, via la phosphofructokinase-1 (
étape 3),
- activation de la glycogénolyse, i.e. activation allostérique directe de la glycogène phosphorylase,
- stimulation de l’AMP-activated protein kinase (AMPK), une kinase maîtresse qui régule le métabolisme en faveur de la production d’énergie.
2. Plusieurs enzymes du cycle de Krebs sont soumises à une régulation allostérique et par rétrocontrôle, en fonction de l’état énergétique de la cellule.
a. La citrate synthase est :
- inhibée par le citrate, produit de la réaction, NADH, excès de pouvoir réducteur, et l'ATP, signe d'énergie abondante,
- activée par l'ADP, signal de demande énergétique.
Remarque : le citrate agit aussi en amont de la glycolyse, comme inhibiteur allostérique de la phosphofructokinase-1, enzyme clé de l’étape 3.
- Cette réaction réduit la formation de fructose-1,6-bisphosphate (F1,6BP), freinant ainsi la glycolyse.
- On observe donc une boucle de rétrocontrôle entre la glycolyse et le cycle de Krebs, permettant à la cellule d’adapter sa production d’énergie selon ses besoins.
b. L'isocitrate déshydrogénase est :
- inhibée par NADH et l'ATP,
- activée par l'ADP et le calcium, en lien avec la contraction musculaire.
c. Le complexe α-cétoglutarate déshydrogénase est :
- inhibé par le NADH, l'ATP et le succinyl-CoA,
- activé par le calcium, en particulier dans les tissus à forte demande énergétique.
Remarque : le calcium, qui augmente lors de la contraction musculaire ou de signaux hormonaux, active aussi la pyruvate déshydrogénase phosphatase et inhibe la pyruvate déshydrogénase kinase, donc active le complexe PDH pour transformer plus de pyruvate en acétyl-CoA, augmentant son entrée dans le cycle de Krebs.
3. Le fonctionnement du cycle nécessite des coenzymes nicotiniques et flaviniques sous forme oxydée.
Il est donc indispensable que NADH et FADH2 cèdent leurs hydrogènes à la chaîne respiratoire, afin de pouvoir participer à nouveau au processus cyclique.
Cycle de Krebs : plateforme métabolique
Réactions anaplérotiques
Les réactions anaplérotiques, du grec ana, vers le haut, et pleroo, remplir, sont des réactions qui permettent de reconstituer les intermédiaires d’un cycle métabolique, ici celui du cycle de Krebs, indépendamment de son déroulement cyclique habituel.
1. Les composés intermédiaires du cycle de Krebs, comme d'autres cycles par ailleurs, doivent être produits en quantité suffisante pour que le cycle se déroule normalement, surtout lorsqu'ils peuvent être utilisés par d'autres voies métaboliques.
a. Théoriquement, tous ces intermédiaires peuvent servir indéfiniment, puisque le cycle est régénératif.
b. En pratique, la quantité d’intermédiaires disponibles devient souvent limitante et il est alors nécessaire de produire ces intermédiaires en plus grande quantité, i.e. groupes acétyles $\ce{R-C(=O)-}$ en provenance des glucides, mais aussi des lipides et des protides, via les réactions anaplérotiques, pour :
- soutenir l’activité du cycle,
- éviter un engorgement en acétyl-CoA non oxydé,
- maintenir l'équilibre métabolique global.
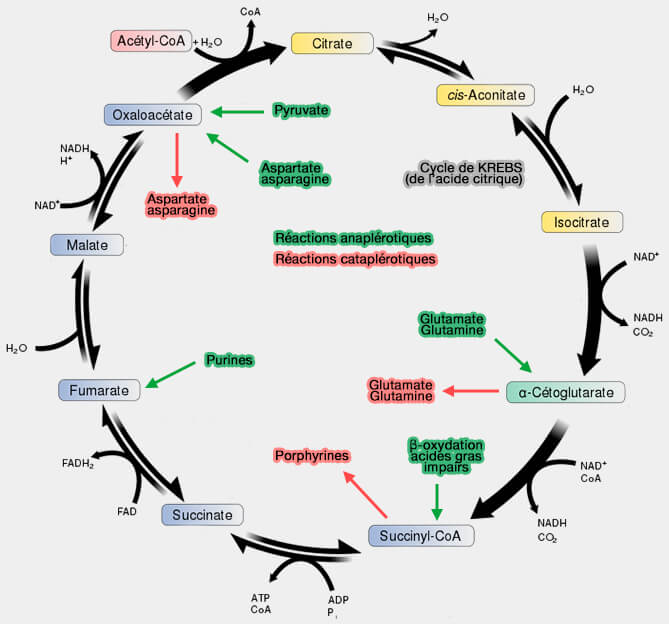
(Figure : vetopsy.fr)
2.. Les réactions anaplérotique les plus importantes produisent de l'oxaloacétate (
- à partir du pyruvate, réaction anaplérotique majeure dans les mitochondries du foie et le rein, par la pyruvate carboxylase (PC) :
$\ce{Pyruvate + HCO3- + ATP}$ $\longrightarrow$ $\ce{Oxaloacétate + ADP + Pi}$
- à partir de l'aspartate, par la transamination via l'aspartate aminotransférase (ASAT ou AST), i.e. réaction réversible interconnectant le métabolisme des acides aminés et celui du cycle de Krebs :
$\ce{Aspartate + α-cétoglutarate}$ $\leftrightharpoons$ $\ce{oxaloacétate + glutamate}$
Remarque : l'asparagine peut aussi être une source car, par la réaction catalysée par l'asparagine synthétase (EC 6.3.5.4) :
$\ce{Aspartate + glutamine + ATP}$ $\leftrightharpoons$ $\ce{Asparagine + glutamate + AMP + Pi}$
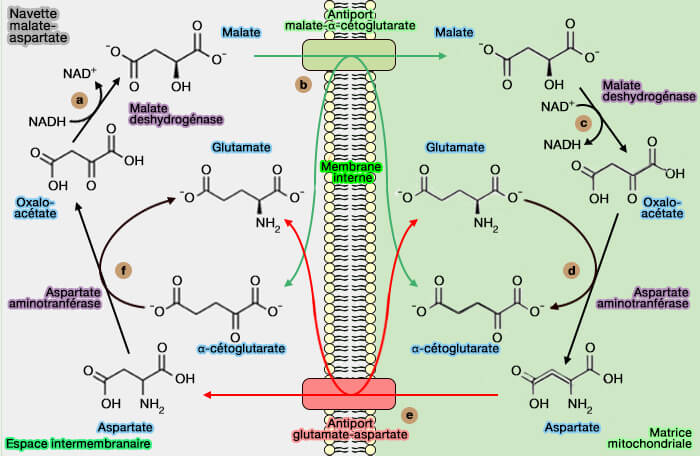
(Figure : vetopsy.fr)
2. Le glutamate peut former de l'α-cétoglutarate par la glutamate déshydrogénase (
$\ce{L-glutamate + H2O + NAD+}$ $\leftrightharpoons$ $\ce{α-cétoglutarate + NH3 + NADH + H+}$
a. La glutamine peut aussi être une source indirecte par la glutaminase (EC 3.5.1.2), puis et ensuite la glutamate déshydrogénase :
$\ce{Glutamine + H2O}$ $\leftrightharpoons$ $\ce{Glutamate + NH3}$
b. Ce double processus permet à la glutamine de nourrir le cycle de Krebs, ce qui est particulièrement important dans les cellules métaboliquement très actives, comme les cellules tumorales.
3. La β-oxydation des acides gras impairs de carbones produit du propionyl-CoA, qui peut être converti en succinyl-CoA, réaction qui s’effectue en trois étapes, catalysées par trois enzymes distinctes.
$\ce{CH3-CH2-CO-S-CoA + HCO3-}$ $\rightarrow$ $\ce{HOOC-CH3-CH3-CO-S-CoA}$

(Figure : vetopsy.fr)
a. Le propionyl-CoA est d'abord métabolisé en (S)-méthylmalonyl-CoA par la propionyl-CoA carboxylase (PCC), i.e. EC 6.4.1.3, une carboxylase à biotine et un ATP.
$\ce{Propionyl-CoA + HCO3- + ATP}$ $\leftrightharpoons$ $\ce{(S)-Méthylamalony-CoA + ADP + P}$
b. Le (S)-méthylmalonyl-CoA, i.e. énantiomère D, ne peut être utilisé tel quel et doit s'épimériser en (L)-méthylmalonyl-CoA, grâce à l'intervention d'une méthylmalonyl-CoA épimérase ou racémase (EC 5.1.99.1).
c. Le (L)-méthylmalonyl-CoA peut alors s'isomériser en succinyl-CoA grâce à la méthylmalonyl-CoA mutase (MUT), i.e. EC 5.4.99.2), avec la cobalamine (vitamine B12) comme cofacteur.
Remarque : le propionyl-CoA peut provenir aussi d'autres sources :
- par oxydation du cholestérol lors de la formation des acides bilaires,
- par oxydation d'acides aminés comme la méthionine, la valine, l'isoleucine et la thréonine,
4. Le fumarate peut être produit :
- dans la dégradation de certains acides aminés, i.e. phénylalanine et tyrosine,
- dans le cycle de l’urée,
- dans le métabolisme des purines à partir de l'adénylosucccinate (
formation de l'AMP et du GMP à partir de l'IMP).
Réactions cataplérotiques
Les réactions cataplérotiques, du grec cata, vers le bas et pleroo, remplir, sont des réactions chimiques qui consomment les intermédiaires des cycles métaboliques, ici du cycle de Krebs.
- L'oxaloacétate est un précurseur des acides aminés comme l'aspartate ou l'asparagine.
- L'α-cétoglutarate est aussi un précurseur de la synthèse d'acides aminés par transamination et produire du glutamate et de la glutamine.
- Le succinyl-CoA est un précurseur des porphyrines (
biosynthèse des porphyrines).
Retour au cycle de Krebs
BiochimieChimie organiqueBioénergétiqueThermodynamique et réactions chimiquesRéactions d'oxydoreduction (rédox)Composés riches en énergieATPADPAMPGTPRespiration cellulaire et production d'ATPPhosphorylation substratCycle de KrebsPhosphorylation oydativeChaîne respiratoireATP synthaseProtidesAcides nucléiquesLipidesGlucidesLipidesEnzymesCoenzymesVitaminesHormonesComposés inorganiques


