Isomérie : stéréoisomérie de configuration
Énantiomères et diastéréoisomères
- Biologie cellulaire et moléculaire
- Biochimie

Les énantiomères et les diastéréoisomères sont des stéréoisomères de configuration, à même formule développée, mais qui nécessitent une rupture de liaison pour passer de l'un à l'autre.
Il existe deux types de stéréoisomérie :
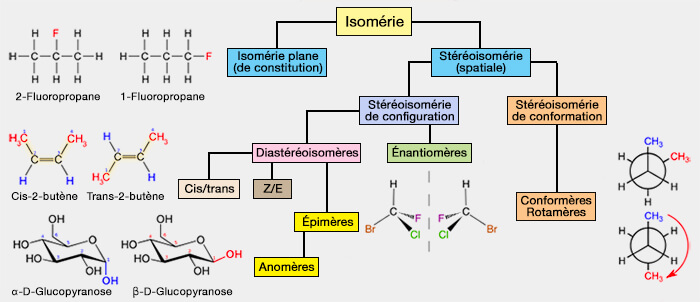
(Figure : vetopsy.fr)

Les modes de représentation de molécules est décrite dans : Cours de chimie organique de G. Dupuis du Lycée Faidherbe de LIlle.
Énantiomères

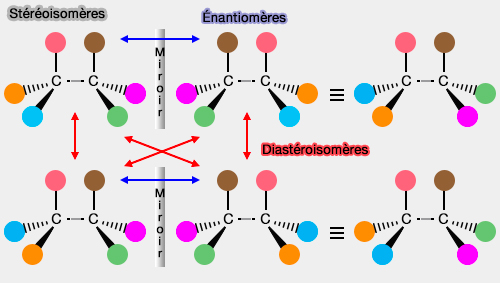
Deux énantiomères sont deux molécules qui sont l'image l’une de l’autre dans un miroir plan, mais qui ne sont pas superposables : ces molécules sont donc chirales.
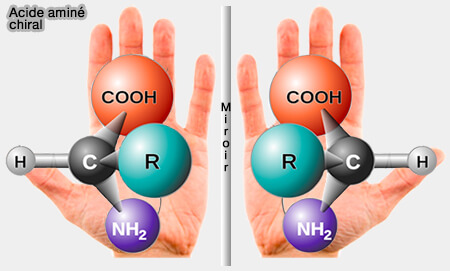
(Figure : vetopsy.fr)
1. Les énantiomères ont les mêmes propriétés physiques, mais leur pouvoir rotatoire diffère.
Quand une molécule est capable de modifier la direction de polarisation d’une onde plane polarisée linéairement, on la dit optiquement active.
La molécule est forcément chirale et on parle de :
- composé dextrogyre (ou +) si la lumière est déviée vers la droite d'un angle α,
- composé lévogyre (ou -) si la lumière est déviée vers la gauche d'un angle -α.
L'angle α est calculé par la loi de Biot :
$\ce{α=[α]_λ^T \times L \times C}$ où :
- $\ce{α_λ ^T}$ est le pouvoir rotatoire de la substance étudiée à la température $\ce{T}$ et à la longueur d'onde $\ce{λ}$,
- $\ce{L}$ est la longueur de la cuve polarimétrique exprimée en dm,
- $\ce{C}$ est la concentration de la solution étudiée en g cm-3.
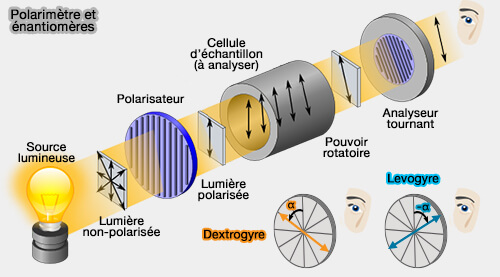
(Figure : vetopsy.fr d'après Kaidor)
Si la déviation est nulle (α=0), deux cas de figures se présentent :
- soit la molécule est achirale,
- soit le mélange est dit racémique, mélange composé des deux énantiomères à part égale, i.e. la racémisation est la conversion d'une solution contenant un seul énantiomère en une solution où les deux sont présents.
Une nomenclature D/L est utilisé pour les sucres, mais à part pour le glycéraldéhyde, elle n'a rien à voir avec le pouvoir rotatoire.
2. Leur propriétés chimiques, donc biologiques ou pharmacologiques, sont souvent, en général, différentes.
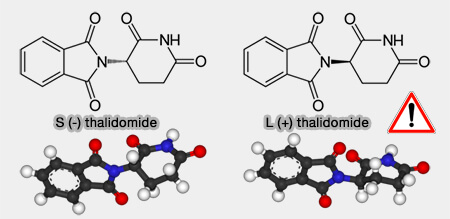
(Figure : vetopsy.fr)
a. On peut citer l'exemple tristement célèbre de la thalidomide qui est racémique.
- La S-thalidomide est la forme bioactive de la molécule, aux effets sédatifs et anti-nauséeux.
- Les énantiomères individuels peuvent se racémiser entre eux grâce à l'hydrogène proche du centre chiral, carbone du cycle glutarimide lié au substituant phtalimide et génèrer la R-thamidomide à effets tératogènes.
La L-dopa entre dans le traitement de la maladie de Parkinson et des dystonies dépendantes de la dopamine.
- Le L-dopa est un précurseur de la dopamine qui traverse la barrière hémato-encéphalique et est captée par les neurones dopaminergiques pour y être transformé en dopamine.
- La D-dopa est biologiquement inactive.
(Figure : vetopsy.fr)
Diastéréoisomères

Deux diastéréoisomères sont deux molécules stéréoisomères qui ne sont pas des énantiomères mais qui ne sont ni superposables, ni image l'une de l'autre dans un miroir.
1. Les diastéréoisomères ont donc des propriétés physiques différentes.
On les classe en :
- 1. isomères cis et trans pour les composés alicycliques, i.e. à la fois aliphatique et cyclique ;
- 2. isomères Z/E pour les chaînes carbonées avec liaison double, mais qui peuvent comportés aussi d'autres double-liaisons ;
- 3. anomères et épimères, i.e. diastéréoisomères essentiellement des glucides ;
- 4. invertomères, dans le cas d'atomes trivalents, comme les trialkyl amines,
- 5. " thréo " et " érythro " (
article de l'université Clermont-Auvergne).
Diastéréoisomérie Z/E
(Figure : vetopsy.fr)
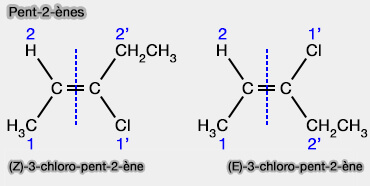
1. La diastéréoisomérie Z/E traduit les relations stériques par rapport à une ou plusieurs doubles liaisons, qu'elles soient entre deux carbones ou entre d'autres atomes.
Les règles de la notation Z/E sont décrites avec la notation CIP.
2. L'exemple sur la figure ci-contre est celui du 3-chloro-pent-2-ène.
Diastéréoisomérie
cis/trans
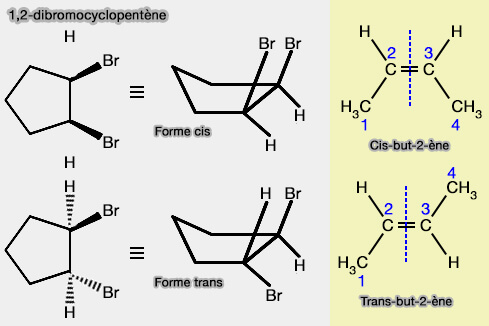
1. La diastéréoisomérie cis/trans est rencontrée pour les substituants des cycles (ou les jonctions de composés polycycliques).
Dans les cycles, on peut ne pas trouver de carbone asymétrique (C*), i.e. la molécule est forcément achirale !
(Figure : vetopsy.fr)
2. Toutefois, on trouve deux représentation spatiales qui sont dues à la présence du cycle.
a. Le composé est dit " cis ", si, par rapport à la chaine principale de la molécule décrite, les principaux groupes fonctionnels sont situés du même côté, i.e. cis-, " ensemble " en latin ;
b. Le composé est dit " trans ", s'ils sont situés de part et d'autre, i.e. trans-, " à travers " en latin.
Remarque : cette notation est quelquefois utilisée pour les doubles liaisons : la différence avec la notation Z/E plus générale est la fait que les substituants doivent être identiques.
Épimères et anomères
Pour les oses en particulier, on définit deux catégories de stéréoisomères.
1. Un épimère est un stéréoisomère dont la configuration diffère d'un centre stéréogène unique.
2. Un anomère est un épimère du carbone hémiacétal dans un saccharide cyclique, i.e. carbone appelé carbone anomérique.


