Lipides
Gouttelettes lipidiques
(Lipid droplets ou LD)
Biogenèse : 2. modèle de nucléation et de bourgeonnement
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Composés organiques
- Protides
- Acides nucléiques
- Glucides
- Lipides
- Coenzymes
- Hormones
- Composés inorganiques
- Composés organiques
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les modèles encore hypothétiques à l'heure actuelle du bourgeonnement des gouttelettes lipidiques (LD) sont basés sur des simulations informatiques, principalement les simulations de dynamique moléculaire (MD) gros grains et le modèle moléculaire.
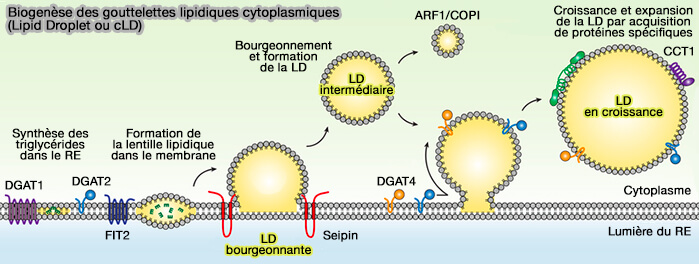
(Figure : vetopsy.fr d'après Walther et coll)
Plusieurs protéines, i.e. la seipine et LDAF1, FIT et Plin3 joueraient un rôle majeur dans le bourgeonnement des gouttelettes lipidiques (
- La seipine, en formant une cage hydrophobe, est essentielle dans ce processus (
structure de la seipine).
- Les périlipines (Plin), en particulier Plin3, à la surface de la LD protègeraient les gouttelettes lipidiques naissantes de la lipolyse.
- Les FIT joueraient aussi un rôle important dans la formation des LD par plusieurs mécanismes en s'associant à des domaines impliqués à la fois dans la synthèse des triglycérides (TG) et dans la biogenèse naissante des LD (
FIT, nucléation et bourgeonnement des LD).
Assemblage des LDAC
La seipine avec LDAF1 (LD assembly factor 1, Ldo45 de la levure) forme un complexe protéique d’assemblage des LD (LDAC ou LD Assembly protein Complexes).
1. La seipine forme des homo-oligomères, de 11 ou 12 sous-unités chez l'homme, i.e. complexe toroïdal d'environ 150 Å de diamètre qui forme une cage hydrophobe (Seipin forms a flexible cage at lipid droplet formation sites 2022).
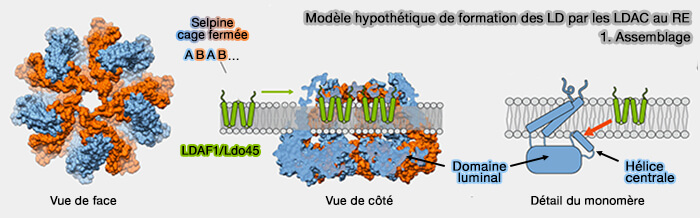
(Figure : vetopsy.fr d'après Whalter et coll)
2. LDAF1 se lierait avec l'hélice centrale du domaine luminal de la seipine (Structure and function of lipid droplet assembly complexes 2023).
a. Ce complexe détermine le site de la formation de la LD dans le réticulum endoplasmique (RE).
D'autres auteurs pensent que c'est FIT2 qui apparaît en premier.
b. La cage de seipine en configuration fermée, i.e. ABAB…, les domaines transmembranaires hydrophobes pouvant changer de conformation, ses hélices hydrophobes ainsi que ceux de LDAF1 génèreraient un espace dans la bicouche relativement pauvre en phospholipides (PL).
1. Accumulation des triglycérides pour former la lentille lipidique
1. Des triglycérides (TG) sont synthétisés au niveau membranaire et la séparation de phases ne se produit pas lorsque la concentration en TG devient supérieure à environ un certain pourcentage en moles (
a. Cette séparation est facilitée par la conformation fermée décrite ci-dessus qui fournit une chambre hydrophobe qui permet peut-être aussi aux TG de diffuser préférentiellement par rapport aux phospholipides.
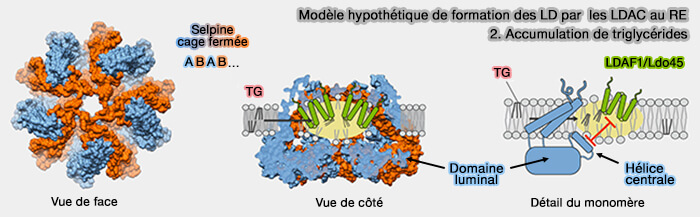
(Figure : vetopsy.fr d'après Whalter et coll)
b. À l'intérieur du complexe, les molécules TG faiblement polaires n'interagissent plus de manière intensive avec les phospholipides (PL) et peuvent ainsi s'auto-associer, conduisant à la nucléation d'une phase huileuse, étape limitante dans la transition de phase nécessaire à la formation de LD.
Les LD se forment à des concentrations de TG plus faibles dans le réticulum endoplasmique (RE) lorsque les LDAC sont présents que sans eux (LDAF1 and Seipin Form a Lipid Droplet Assembly Complex 2019).
c. Les domaines transmembranaires (TM) pourraient faciliter ce processus en se liant au TG comme proposé par certaines simulations moléculaires (

La seipine permettrait les interactions des TG, catalysant ainsi la séparation de phase, la formation de lentilles et la croissance des LD.
2. Au fur et à mesure que la lentille TG se développe, LDAF1, par l'accumulation de lipides, se libère de la seipine au sein du LDAC et se déplace vers la surface de la LD en formation.
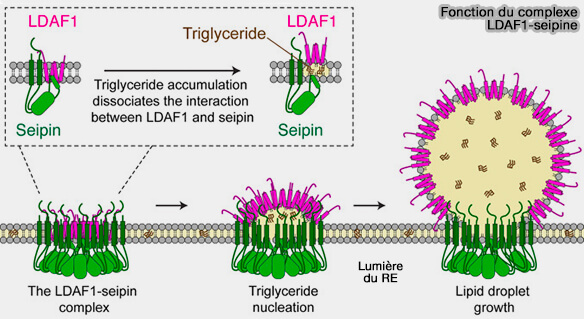
(Figure : vetopsy.fr d'après Chung et coll)
a. Cette redistribution de LDAF1 pourrait réduire la tension superficielle des LD, favorisant ainsi un bourgeonnement et une croissance efficace (The Physics of Lipid Droplet Nucleation, Growth and Budding 2016).
- La séquestration de LDAF1 sur les LD pourrait aussi empêcher la formation de nouvelles LD une fois qu'une première vague de biogenèse se produit.
- Le pool de LDAF1 non associé à la seipine du RE est réduit, i.e. les niveaux de LDAF1 pourraient être en corrélation avec le nombre de LD cellulaires.
b. Les fortes interactions des sous-unités luminales de la seipine fournissent un ancrage moléculaire qui maintient la connexion du LD en formation avec le réticulum endoplasmique (RE).
c. En outre, les résidus conservés et chargés positivement à l’extrémité des extrémités N- et C-terminales exposés au cytosol interagissent avec le feuillet cytosolique.
- Elles protègent la structure des parties hydrophobes de la membrane.
- Elles contraignent le col de la LD en formation, permettant le bourgeonnement des LD à partir du RE par une augmentation de l'angle de contact entre la gouttelette et la bicouche du RE (
démouillage ou dewetting).
2. Bourgeonnement de la LD
1. À mesure que la LD en formation grossit, l'oligomère seipine peut s'ouvrir vers le cytoplasme, avec toutes les sous-unités dans la conformation A, et ainsi libérer la lentille pour générer une LD bourgeonnante (Structure and function of lipid droplet assembly complexes 2023).
Les domaines transmembranaires (TM) de la cage de seipine pourraient s'incliner davantage par rapport au centre du dôme pour s'adapter aux LD en croissance grâce à la région de commutation et ses interactions avec les TM, augmentant ainsi la flexibilité du côté cytoplasmique.
Les mutants dans la région de commutation semblent conduire à un complexe seipine qui ne peut pas maintenir un col resserré à la jonction RE/LD, mais se dissocie et intègre davantage de sous-unités seipine, formant finalement les structures annulaires de grand diamètre.
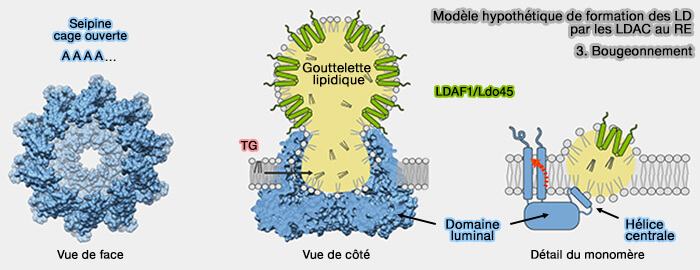
(Figure : vetopsy.fr d'après Whalter et coll)
2. Au cours de ce processus, davantage de molécules LDAF1, ce qui diminue leur pool libre (cf. plus haut).
3. Des protéines sélectionnés ciblent la surface croissante des LD, pendant que d'autres protéines du RE sont probablement exclues (Identification of two pathways mediating protein targeting from ER to lipid droplets 2022).
D'autres protéines encore ciblent les surfaces LD à des moments ultérieurs.
- soit à partir des MCS RE-LD (Triacylglycerol Synthesis Enzymes Mediate Lipid Droplet Growth by Relocalizing from the ER to Lipid Droplets 2013),
- soit à partir du cytosol (Determinants of Endoplasmic Reticulum-to-Lipid Droplet Protein Targeting 2020).
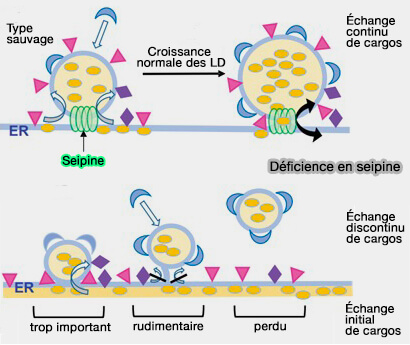
(Figure : vetopsy.fr d'après Salo et coll)
4. D'autres protéines peuvent être impliquées dans la définition de l'étape initiale de bourgeonnement et de l'expansion des LD, car les LD et le réticulum endoplasmique (RE) restent en contact même lorsque la seipine est absente (Seipin regulates ER–lipid droplet contacts and cargo delivery 2016 et Seipin is required for converting nascent to mature lipid droplets 2016 et Seipin Deficiency as a Model of Severe Adipocyte Dysfunction: Lessons from Rodent Models and Teaching for Human Disease 2022).
a. En absence de seipine, les gouttelettes lipidiques nouvellement formées sont de taille très réduite, ce qui montre une incorporation faible d'acides gras, alors même que leur synthèse est normale (
Ces mini-gouttelettes possèdent des protéines différentes à leur surface, ce qui pourrait altérer leur capacité à stocker les graisses.
b. Lorsque certaines de ces minuscules gouttelettes se détachent dans le cytosol, elles entrent dans une autre voie d’expansion des gouttelettes lipidiques, qui les transforme en gouttelettes lipidiques anormalement grosses (
Et les gouttelettes contenant des esters de cholestérol (CE) ?
Toutes les études de la biogenèse des gouttelettes lipidiques se sont concentrées sur les LD contenant des triglycérides (TG). Or, la seipine se retrouve aussi au niveau des MCS RE/LD des LD contenant des esters de cholestérol ou CE (Membrane Curvature Catalyzes Lipid Droplet Assembly 2020).

Vous pouvez lire : Seipin-still a mysterious protein? (2023), car cet article fait le point des connaissances actuelles.
L'assemblage pourrait être différent à cause des propriétés physico-chimiques des CE, mais les études paraissent contradictoires (Lipid Droplet Nucleation 2021).
- La seipine n'a pas pu être localisée, ni au niveau des CE-LD de la levure, ni sur celles des LD avec des esters de rétinyle (Retinyl esters form lipid droplets independently of triacylglycerol and seipin 2021).
- Par contre, des simulations ont montré qu'elle joue le même rôle que dans les TG-LD, avec quelques différences (Seipin concentrates distinct neutral lipids via interactions with their acyl chain carboxyl esters 2022 et Lipid Droplet Biogenesis: a mystery “unmixing”? 2022).
3. Expansion des goutellettes lipidiques
BiochimieChimie organiqueBioénergétiqueProtidesGlucidesLipidesAcides grasLipides vraisLipides vrais simplesLipides vrais complexesLipoïdesCholestérolGlycéridesPhospholipidesTrafic non vésiculaire et LTPDigestion et absorption entérocytaire des lipidesLipoprotéinesApolipoprotéinesGouttelettes lipidiques (LD)EnzymesCoenzymesVitaminesHormonesComposés inorganiquesTransport membranaireMoteurs moléculairesVoies de signalisation


