Glucides : dégradation du glucose
Glycolyse ou voie d'Embden-Meyerhof
Fermentations
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

La glycolyse produit du pyruvate, qui peut être transformé en divers composés par fermentation, permettant la régénération du NAD+ nécessaire à la poursuite de la glycolyse en absence d’oxygène.
La production d'énergie à partir du glucose est essentiellement assurée par la voie d'Embden-Meyerhof.
$\ce{Glucose + 2 NAD+ + 2 ADP + 2 Pi}$ $\longrightarrow$ $\ce{pyruvate + 2 NADH + 2 H+ + 2 ATP + 2 H2O}$
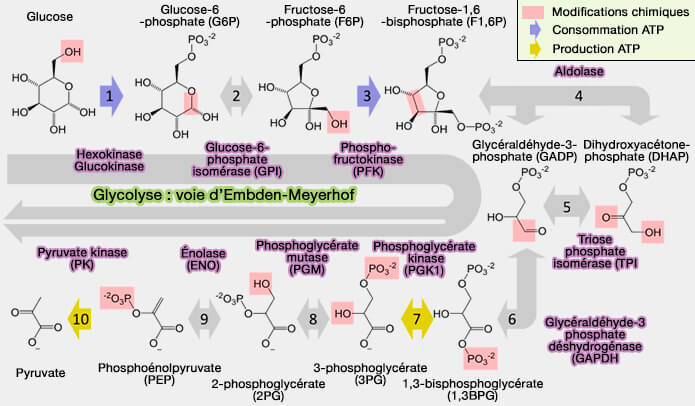
(Figure : vetopsy.fr d'après Thomas Shafee)
La glycolyse, qui se déroule entièrement dans le cytosol, est divisée en deux phases principales :
- une phase dite préparatoire qui conduit du glucose à deux glycéraldéhyde-3-phosphate (G3P), avec consommation d'ATP,
- une phase finale, oxydo-réduction couplée à la formation du pyruvate et d'ATP.
Devenir du pyruvate en anaérobiose
1. En aérobiose, avec $\ce{O2}$, le pyruvate est oxydé dans les mitochondries.
Il est converti en acétyl-CoA par le complexe pyruvate déshydrogénase (PDH), puis entre dans le cycle de Krebs et alimente la chaîne respiratoire de transport d'électrons, pour une production efficace d’ATP par l'ATP synthase.
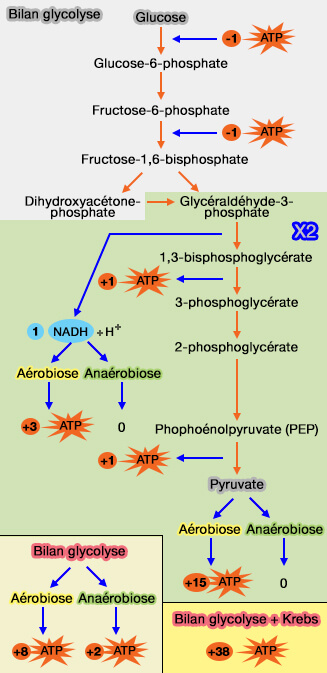
(Figure : vetopsy.fr)
2. En anaérobiose, sans $\ce{O2}$ ou lorsque la chaîne respiratoire ne peut plus fonctionner, le pyruvate ne peut plus être oxydé : il subit alors des fermentations, transformations différentes selon la nature des enzymes présentes dans la cellule.
a. Chez l'homme, la seule fermentation est la fermentation lactique qui conduit à l'acide lactique (lactate), notamment dans les muscles soumis à un effort intense.
b. Chez les micro-organismes, d'autres fermentations sont possibles :
- la fermentation alcoolique, la plus fréquente, qui conduit à l'éthanol,
- d'autres fermentations qui conduisent à différents acides (propionique, succinique, butyrique ou citrique) ou à l'acétone (
fermentations), fréquentes notamment dans le microbiote intestinal.
Remarque : certains auteurs utilisent le terme de fermentation uniquement pour les processus industriels, ce qui ne sera pas le cas dans ce site.
Fermentation et
acidose lactique
1. La fermentation lactique, i.e. en l'absence d'une chaîne respiratoire de transport d'électrons, conduit à la réduction du pyruvate en lactate $\ce{CH3CH(OH)COO-}$, et à l'oxydation de $\ce{NADH}$ en $\ce{NAD+}$.
$\ce{Pyruvate + NADH + H+}$ $\leftrightharpoons$ $\ce{L-lactate + NAD+}$
2. L'acidose lactique fait intervenir le même processus quand le pyruvate, suite à un problème du métabolisme oxydatif, ne peut être converti en acétyl-CoA pour entrer dans le cycle de Krebs.
Lactate déshydrogénase
(LDH ou LD)
La lactate déshydrogénase (LDH ou LD), EC 1.1.1.27, catalyse la conversion réversible entre le pyruvate et le lactate, avec régénération du NAD+, indispensable à la glycolyse.
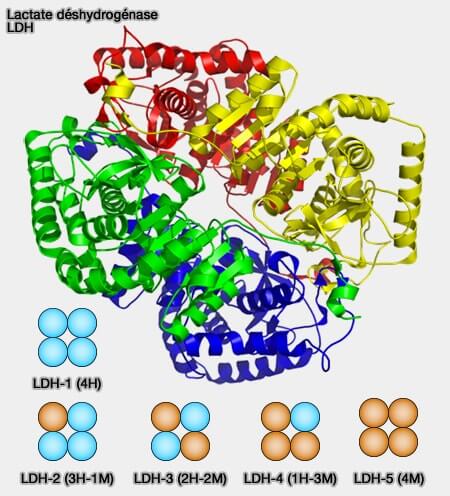
1. La lactate déshydrogénase LDH est un tétramère formé à partir de différentes combinaisons de sous-unités codées par des gènes distincts.
-
Cycle de l'alanine (cycle de Cahill) et cycle de Cori
(Figure : vetopsy.fr)
a. LDH-A (ou LDH-M , M pour Muscle) favorise la production de lactate à partir de pyruvate.
- Elle est active quand la cellule a besoin de régénérer du NAD+ pour maintenir la glycolyse.
- Elle n'est pas inhibée par de fortes concentrations de pyruvate.
b. LDH-B (ou LDH-H, H pour Heart, cœur) favorise la production de pyruvate à partir de lactate, utilisé ensuite dans la respiration mitochondriale.
- Elle est active dans les tissus où le métabolisme aérobie prédomine.
- Elle est inhibée par de fortes concentrations de pyruvate.
2. Les deux sous-unités, i.e. LDH-H et LDH-M, peuvent s’assembler en tétramères pour former 5 isoenzymes différents, présents dans des tissus spécifiques :
- LDH-1 (4H), dans le coeur, dans les globules rouges et dans le cerveau ;
- LDH-2 (3H1M), dans le système réticulo-endothélial, donc dans le sérum
- LDH-3 (2H2M), dans les poumons,
- LDH-4 (1H3M), dans les reins, le placenta et le pancréas,
- LDH-5 (4M), dans le foie et les muscles striés.
Remarque : on trouve deux autres sous-unités dans les testicules des mammifères.
a. LDH-C est adaptée au métabolisme énergétique spécifique des spermatozoïdes.
- Le spermatozoïde a besoin d’une grande quantité d’énergie (ATP) pour assurer sa motilité.
- Contrairement à d’autres cellules, les spermatozoïdes utilisent principalement la glycolyse anaérobie.
b. LDHBx, forme alternative du gène LDHB, produite par épissage alternatif, est spécifique des peroxysomes des testicules (Peroxisomal lactate dehydrogenase is generated by translational readthrough in mammals 2014).
LDHBx pourrait pourrait participer à un métabolisme énergétique secondaire, notamment à la régulation du redox ou du métabolisme lipidique dans les testicules.
Rôles de la LDH
Glycolyse anaérobie
1. Au cours d'un exercice intense, les besoins énergétiques de la contraction musculaire augmentent fortement, ce qui entraîne une hydrolyse massive de l’ATP.
a. Cette réaction libère des protons ($\ce{H^+}$), contribuant à l’acidification du milieu intracellulaire (
$\ce{ATP^4- + H2O}$ $\longrightarrow$ $\ce{ADP^3- + HPO4^2− +H+}$
b. Normalement, l’ATP est régénéré par la phosphorylation oxydative dans les mitochondries par le cycle de Krebs.
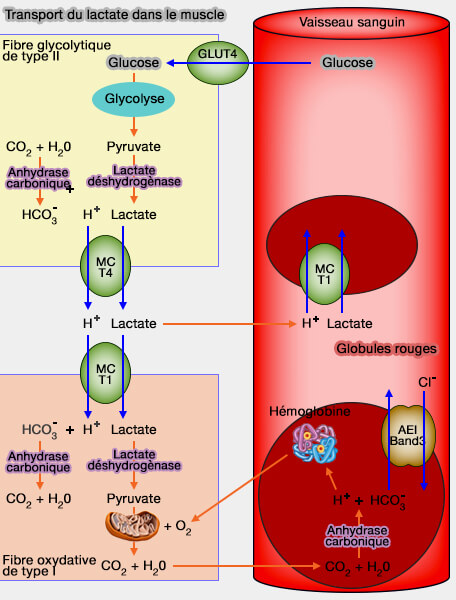
(Figure : vetopsy.fr d'après université de Montpellier)
2. Lorsque la demande dépasse les capacités mitochondriales, notamment en cas de manque d’oxygène, le pyruvate issu de la glycolyse ne peut plus entrer dans le cycle de Krebs et produire de l'ATP par la phosphorylation oxydative.

Les cellules doivent recourir à la glycolyse anaérobie, une voie plus rapide mais moins efficace.
a. Le pyruvate est alors converti en lactate par la lactate déshydrogénase (LDH), une réaction qui ne sert pas à produire de l’énergie directement, mais qui permet de régénérer le $\ce{NAD+}$ à partir du $\ce{NADH}$.
- Cette régénération est essentielle pour maintenir la glycolyse active et donc, la production d’ATP en condition anaérobie.
- En effet, la glycolyse nécessite du $\ce{NAD^+}$ dans son étape 6, i.e. lors de l’oxydation du glycéraldéhyde-3-phosphate, i.e. sans régénération de ce cofacteur, la voie s’arrête, stoppant ainsi la production d’ATP.
b. Toutefois, cette stratégie présente une contrepartie, i.e. l’hydrolyse accrue d’ATP et la poursuite de la glycolyse génèrent une quantité importante de protons, contribuant à une acidification intracellulaire progressive.
- Le lactate n’est pas directement responsable de l’acidité, mais son accumulation reflète une production accrue de protons par la glycolyse anaérobie et l’hydrolyse de l’ATP.
- Par ailleurs, lorsque le potentiel d’oxydoréduction intracellulaire devient inférieur à –0,20 V, ce qui se produit notamment dans un muscle privé d’oxygène (anoxie) à cause de l'accumulation de NADH (réducteur) et la diminution de NAD+ (oxydant), les conditions deviennent suffisamment réductrices pour que la conversion du pyruvate en lactate par la LDH soit thermodynamiquement favorisée.
3. Lorsque l'accumulation de lactate devient excessive, elle contribue à une acidose métabolique, observée dans diverses situations cliniques :
- fatigue musculaire sévère,
- lésions musculaires traumatiques,
- infarctus.
Cycle de Cori
Le cycle de Cori, du nom de Carl Ferdinand Cori et Gerty Theresa Cori, est un mécanisme métabolique qui permet à l’organisme, en particulier pendant un effort intense ou en situation d’hypoxie (manque d’oxygène), de recycler le lactate produit par les muscles et de maintenir la production d’énergie.
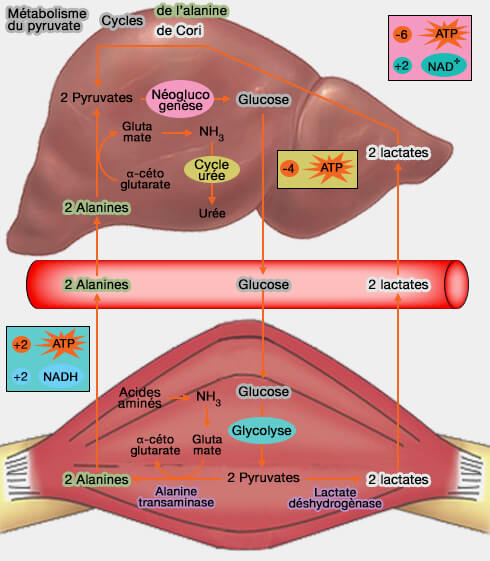
(Figure : vetopsy.fr)
1. Le lactate produit dans le muscle est libéré dans le sang et transporté jusqu’au foie.
a. Là, il est reconverti en pyruvate par la même réaction qui se produit dans le mucle.
$\ce{L-lactate + NAD+}$ $\leftrightharpoons$ $\ce{Pyruvate + NADH + H+}$
b. Le pyruvate est transformé en glucose par la voie de la glunéocogenèse.
$\ce{2Pyruvate + 4ATP + 2GTP + 2NADH ATP + 6H2O}$
$\longrightarrow$ $\ce{Glucose + 4ADP + 2GDP + 6Pi + 2NAD+ + 2H+}$
- Le coût énergétique est élevé par la consommation de 6 molécules énergétiques, 4 ATP/2 GTP pour régénérer 1 seul glucose.
- Cela explique pourquoi ce cycle est transitoire, i.e. il soulage temporairement le muscle, mais épuise les réserves hépatiques s'il devait se prolonger.
2. Un autre cycle faisant intervenir le pyruvate est le cycle de l'alanine, cycle de Cahill ou cycle glucose-alanine (
| Caractéristique | Cycle de Cori | Cycle de Cahill (glucose-alanine) |
|---|---|---|
| Transporté vers le foie | Lactate | Alanine |
| Source de pyruvate | Glycolyse (pyruvate ➞ lactate) |
Glycolyse + transamination (pyruvate + glutamate ➞ alanine) |
| Rôle principal |
|
Transporter l'ammoniac vers le foie pour détoxification |
| Déchet azoté produit | Aucun | Urée |
| Conditions d'activation |
|
|
| Consommation hépatique | 6 ATP pour 1 glucose (gluconéogenèse) |
6 ATP pour 1 glucose + coût du cycle de l'urée |
Rôles dans le métabolisme aberrant du pyruvate
LDH joue un rôle essentiel dans le métabolisme des cellules cancéreuses.

L'effet Warburg est décrit dans un chapitre spécifique.
- Les cellules cancéreuses produisent leur énergie grâce à un fort taux de glycolyse suivie d'une fermentation d'acide lactique (anaérobie) dans le cytosol.
- Les taux de glycolyse des cellules tumorales malignes, au développement très rapide, sont multipliés par 200 fois, même si l'oxygène est abondant.
Fermentation alcoolique
La fermentation alcoolique, chez certains micro-organismes comme les levures, conduit à l'éthanol, $\ce{CH3-CH2-OH}$.
$\ce{Pyruvate}$ $\leftrightharpoons$ $\ce{acétaldéhyde + CO2 + NADH + H+}$ $\leftrightharpoons$ $\ce{éthanol + NAD+}$
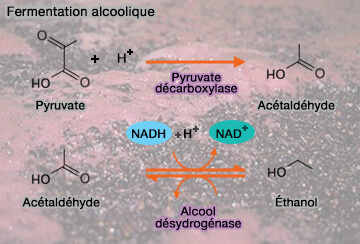
(Figure : vetopsy.fr)
Cette réaction se fait en deux étapes.
1. La décarboxylation du pyruvate en acétaldéhyde (éthanal) et $\ce{CO2}$, est catalysée par une pyruvate décarboxylase (EC 4.1.1.1), dont la coenzyme est la thiamine pyrophosphate (TPP or ThPP, thiamine diphosphate ThDP ou cocarboxylase.
2. La réduction de l'acétaldéhyde en éthanol et oxydation du $\ce{NADH + H+}$ en $\ce{NAD+}$ est catalysée par l'alcool déshydrogénase (EC 1.1.1.1).
L'acétaldéhyde (éthanal) sert aussi d'intermédiaire aux biosynthèses de l'acétyl-CoA :
- lors de la décarboxylation de l'acide pyruvique par la pyruvate déhydrogénase (PDH) qui nécessite la thiamine pyrophosphate (TTP) à laquelle elle se combine pour former un hydroxyéthyl-TPP (HETPP).
- lors de son oxydation par le $\ce{NAD+}$ avec la CoA par l'acétaldéhyde déshydrogénase.
Bilan énergétique des fermentations
En anaérobiose, la réoxydation du $\ce{NADH + H+}$ en $\ce{NAD+}$ ne permet pas de récupération d'énergie sous forme d'ATP.
Le bilan énergétique global de la glycolyse reste donc limité qu'à 2 molécules d'ATP par molécule de glucose, produites lors de la conversion du glucose en pyruvate, étape commune à l'aérobie et à l'anaérobie.
$\ce{Glucose + 2 NAD+ + 2 ADP + 2 Pi}$ $\longrightarrow$ $\ce{2 pruvate + 2 NADH + 2 H+ + 2 ATP + 2 H2O}$


