Glucides
Nucléotides-oses
Biosynthèse des osides
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les nucléotides-oses (nucleotide sugars en anglais) sont des nucléotides liés à des oses qui, entre autres, interviennent dans la biosynthèse des osides.
Les nucléotides-oses interviennent :
- comme donneur d'unités glycidiques lors de :
- comme donneur d'unités glycidiques lors de :
- la biosynthèse des osides,
- la glucurono-conjugaison traitée avec les acides uroniques,
- la glycosylation des protéines, traitée dans des chapitres spécifiques.
Remarque : l'autre donneur d'unités glucidiques est le dolichol phosphate.
Biosynthèse des osides par les nucléotides-oses
Pour transférer une unité glycosyle d'un donneur à un accepteur, il faut une réaction exergonique qui est effectuée le plus souvent par les nucléotides-oses.

Ces réactions sont catalysées par des glycosyltransférases (EC 2.4.) que vous pouvez étudier dans Glycosyltransferases and Glycan-Processing Enzymes, ou plus succinctement dans glycosyltransférases. Nous donnerons succinctement des exemples en nous focalisant sur les osides les plus importants, en particulier animaux !
Biosynthèse des oligosaccharides
Lactose
Biosynthèse par les oses
Le lactose, i.e. β-D-galactopyranosyl(1→4)D-glucopyranose est synthétisé grâce à l'UDP-galactose (UDP-Gal), selon la réaction :
$\ce{UDP-α-D-Galactose + D-Glucose}$ $\leftrightharpoons$ $\ce{Lactose + UDP + H(+)}$
La lactose synthase (EC 2.4.1.22), enzyme qui catalyse cette réaction, est un complexe protéique.
1. La β4-galactosyltransférase-1 ou β-1,4-galactosyltransférase ou UDP-galactose β-N-acétylglucosaminide β-1,4 galactosyltransférase-1 (EC 2.4.1.38 ou 2.4.1.90) est une enzyme retrouvée dans de nombreux tissus de mammifères où elle catalyse normalement la formation de liaisons galactose/β-1,4-N-acétylglucosamine (GlcNAc) dans les chaînes glucidiques des glycoprotéines.
- Opérant seule, la β4-galactosyltransférase-1 catalyse très faiblement la synthèse du lactose car elle se lie peu au glucose.
- En effet, la galactosyltransférase ajoute habituellement du galactose à la N-acétylglucosamine (GlcNAc), qui n'est pas l'activité catalytique nécessaire à la synthèse du lactose dans la glande mammaire.
$\ce{UDP-Galactose + N-acétylglucosamine}$ $\leftrightharpoons$ $\ce{N-acétyllactosamine + UDP}$
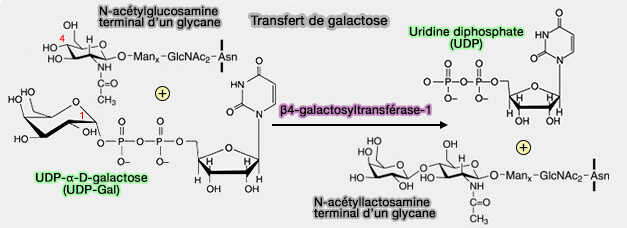
(Figure : vetopsy.fr)
2. L'α-lactalbumine se lie à la β4-galactosyltransférase-1 pour modifier sa spécificité de substrat de la galactosyltransférase de la N-acétylglucosamine au galactose, rendant ainsi possible la synthèse du lactose dans la glande mammaire.
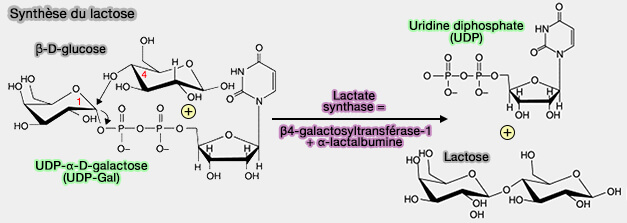
(Figure : vetopsy.fr)
Fermentation ou acidose lactique
La fermentation lactique conduit à la réduction du pyruvate en lactate $\ce{CH3CH(OH)COO-}$, et à l'oxydation de $\ce{NADH}$ en $\ce{NAD+}$.
$\ce{Pyruvate + NADH + H+}$ $\leftrightharpoons$ $\ce{L-lactate + NAD+}$
Saccharose
Le saccharose, i.e. $\ce{Glucose-O-fructose}$, est l'oligosaccharide le plus abondant chez les végétaux supérieurs.
1. La première réaction, catalysée par la saccharose-6-phosphate synthase (EC 2.4.1.14) fait intervenir :
- le fructose-6-phosphate qui apparaît dans la réaction 2 de la glycolyse ou dans l'hydrolyse des esters phosphoriques de la gluconéogenèse,
- l'UDP-glucose.
$\ce{UDP-Glucose + Fructose-6-P}$ $\leftrightharpoons$ $\ce{Saccharose-6-P + UDP}$
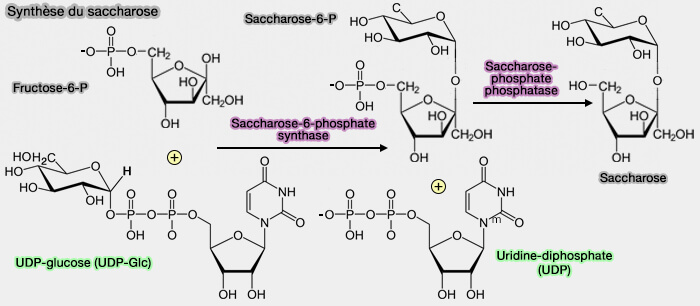
(Figure : vetopsy.fr)
2. L'hydrolyse du saccharose-6-phosphate en saccharose est effectuée par la saccharose-phosphate phosphatase (EC 3.1.1.24) qui favorise la réaction dans le sens de la synthèse du saccharose.
Remarque : il existe bien d'autres oligosaccharides végétaux.
Biosynthèse des polysaccharides
Généralités
1. Les polysaccharides sont synthétisés selon l'équation :
$\ce{UDP-ose + (Ose)_n}$ $\leftrightharpoons$ $\ce{(Ose)_{n+1} + UDP}$
a. Le transfert d'un reste osyle sur une chaîne préformée, catalysé par les glycosyltransférases, forme une chaine linéaire.
Ces restes osyles sont la plupart du temps des UDP-glucose, i.e. pour le glycogène, l'amidon et la cellulose.
b. Par la suite, des enzymes dites de ramification ou branchantes ramifient les chaînes (
2. Cette synthèse nécessite une amorce, i.e. la glycogénine pour le glycogène.
Cas particuliers
1. La synthèse de l'amidon est très complexe et nécessite pas moins de 12 enzymes (Biochemistry and Genetics of Starch Synthesis 2010).
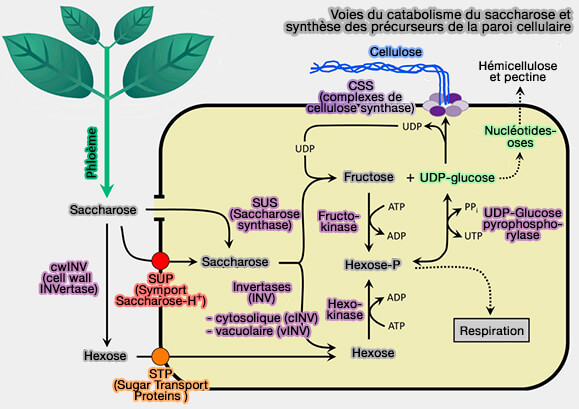
(Figure : vetopsy.fr d'après Verbančič et coll)
2. La cellulose est synthétisée par des complexes de cellulose synthase (CESA), appelés CSC, qui sont assemblés dans l'appareil de Golgi, puis délivrés à la membrane plasmique (PM) où ils synthétisent activement la cellulose (The Cell Biology of Cellulose Synthesis 2014 et The Regulation of Cellulose Biosynthesis in Plants 2019).
- Les CSC se retrouvent dans des structures protéiques hexamériques, d'environ 25 nm de diamètre, appelées RTC (Rosette Terminal Complexes).
- Le substrat des CESA est l'UDP-glucose (Carbon Supply and the Regulation of Cell Wall Synthesis 2018), synthétisé à partir de la voie cytosolique des invertases, i.e. EC 3.2.1.26 (Cytosolic invertases contribute to cellulose biosynthesis and influence carbon partitioning in seedlings of Arabidopsis thaliana 2018).
Biosynthèse des hétérosides
1. Les glucuronides sont des hétérosides éliminés dans l'urine chez les mammifères qui permettent une détoxication de l'organisme (
$\ce{UDP-glucose}$ $\longrightarrow$ $\ce{UDP-acide-glucuronique + R-X-H}$ $\longrightarrow$ $\ce{Glucuronide + UDP}$
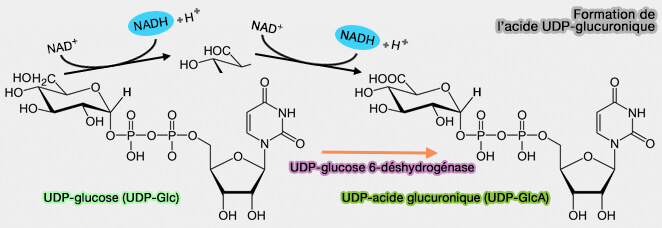
(Figure : vetopsy.fr)
2. Chez les végétaux, la combinaison se fait entre l'ose et une aglycone hydroxylée, i.e. alcool ($\ce{R-OH}$) ou phénol ($\ce{-C6H5-OH}$), le reste osyle étant transféré à partir d'un nucléotide-ose.
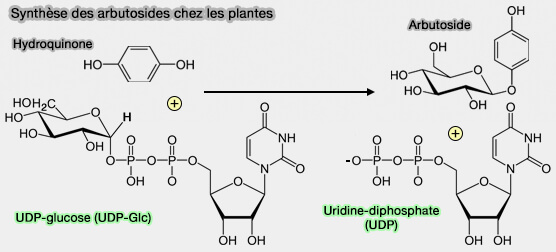
(Figure : vetopsy.fr)
Biosynthèse des osides n'utilisant pas les nucléosides-oses
1. La biosynthèse des osides peut également avoir lieu directement par le saccharose, en particulier chez les plantes et les microorganismes, qui sert de donneur de fructose.
Les microrganismes peuvent aussi utiliser des osyl-phosphates.
2. Les osyl-diphosphates, catalysés par des phosphorylases peuvent tranférer un 5-phosphoribosyle, i.e. 5-phosphoribosyl pyrophosphate sur une base purique ou pyrimidique, conduisant aux nucléotides.
$\ce{5-Phosphoribosyl diphosphate + Adénine}$ $\longrightarrow$ $\ce{AMP + P-Pi}$


