Glucides
Osides : liaison glycosidique et holosides
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les osides sont des polymères d'oses liés par des liaisons glycosidiques.
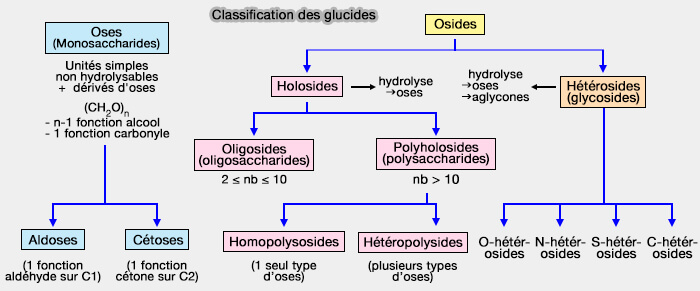
(Figure : vetopsy.fr)

Nous ne détaillerons pas tous les glucides, leur structure et leurs propriétés. Vous pouvez lire : Les glucides : définitions, importance biologique et classification.
Liaison glycosidique
Une liaison glycosidique (ou osidique) est une liaison chimique covalente.
1. Le groupement réducteur est un hydroxyle ($\ce{-OH}$) de la fonction alcool du carbone anomérique d'un ose, i.e. C1 chez les aldoses et numéro C2 des cétoses.
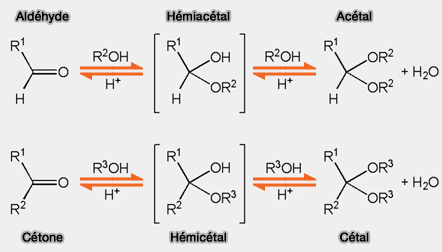
(Figure : vetopsy.fr)
a. Le carbone anomérique est le carbone dérivé du groupe carbonyle ($\ce{C=0}$) de la forme à chaîne ouverte de la molécule glucidique.
b. Un hémiacétal (ou un hémicétal) est un composé résultant de l'addition d'un alcool, ($\ce{R-OH}$), à un aldéhyde, $\ce{R-CH=O}$, ou à une cétone, $\ce{R-C(=O)-R'}$).
- Hémi désigne le fait qu'un seul alcool ($\ce{R_{1,2,3}-C-OH}$) a été ajouté au groupe carbonyle ($\ce{C=0}$).
- L'acétal ou le cétal en comporte deux (
acétal).
2. La formation d’une liaison glycosidique résulte de la réaction entre le groupe hydroxyle hémiacétalique du carbone anomérique d’un ose et un groupement nucléophile d’une autre molécule (par exemple $\ce{-OH}$, $\ce{-NH2}$, $\ce{-SH}$ ou un carbone activé)
a. Dans les liaisons glycosidiques entre oses (holosides), cette liaison glycosidique peut lier le carbone hémiacétalique d'un ose à plusieurs groupes fonctionnels d'un autre ose et former un holoside.
- Lors de la liaison à l'$\ce{-OH}$ hémiacétalique en C1, le diholoside sera non réducteur.
- Lors de la liaison à une fonction alcool primaire ($\ce{-CH2OH}$) en C6 ou une fonction alcool secondaire $\ce{RR'CHOH}$ en C2, C3 et C4, le diholoside sera réducteur car sa fonction hémiacétalique est libre et la mutarotation est possible.
Remarque : La liaison glycosidique bloque l'anomérie de l'ose en position α, i.e. si le groupe hydroxyle ($\ce{-OH}$) anomérique et le groupe $\ce{CH2OH}$ terminal sont de part et d’autre du cycle, ou β, s’ils sont du même côté.
Les méthodes d'étude de la liaison glycosidique sont traitées dans : Les glucides.
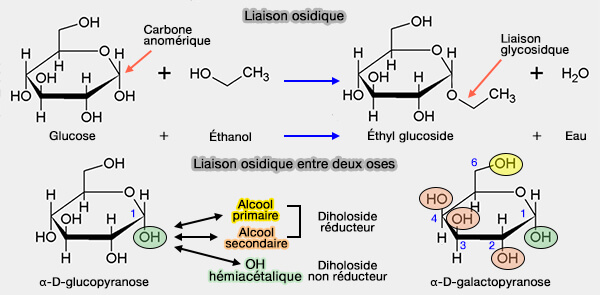
(Figure : vetopsy.fr)
b. Le groupement acide peut être aussi l'hydrogène libre ($\ce{-H}$) d'une molécule autre qu'un ose (hétérosides) i.e. $\ce{R-O+H}$ est appelé aglycane, et selon l’atome impliqué dans la liaison avec le carbone anomérique, et par ordre de fréquence biologique eput être :
- un alcool ($\ce{R-OH}$), i.e. formation d’un O-hétéroside correspondant à une liaison O-glycosidique, comme un O-glucoside si l’ose est un glucose (
O-glycosylation),
- une amine ($\ce{R-NH2}$), i.e. formation d’un N-hétéroside correspondant à une liaison N-glycosidique, appelé aussi glycosylamine, comme un N-glucoside si l'ose est un glucose (
N-glycosylation),
- un thiol ($\ce{R-SH}$), i.e. formation d'un S-hétéroside correspondant à une liaison S-glycosidique, comme un S-glucoside si l'ose est un glucose,
- un carbone d'une autre molécule plus rarement, i.e. formation d'un C-hétéroside correspondant à une liaison C-glycosidique (ou composé C-glycosylé), comme un C-glucoside si l'ose est un glucose (
C-glycosylation).
Remarque : selon l'IUPAC (International Union of Pure and Applied Chemistry), l'appellation " C-glycoside " est un terme impropre. Le terme préféré est " composé C-glycosylé ".
3. Lors de la cyclisation d’un ose, le carbone issu du groupe carbonyle devient le carbone anomérique et la configuration α ou β dépend alors de l’orientation du substituant porté par ce carbone.
- Dans les liaisons O-glycosidiques entre oses (disaccharides et polysaccharides), cette configuration est déterminante pour la structure et les propriétés du polymère.
- Dans certaines liaisons biologiques, ans certaines liaisons biologiques, la configuration est pratiquement toujours β, comme dans les liaisons N-glycosidiques des nucléosides ou des glycoprotéines.
Remarque : dans les nucléosides, la base azotée est liée au carbone anomérique du ribose ou du 2'-désoxyribose par une liaison β-N-glycosidique.
En revanche, les groupes phosphate des nucléotides sont liés au oses par des liaisons phosphoester et non par des liaisons glycosidiques.
Nomenclature
Les conventions de la nomenclature des osides sont relativement complexes.
1. Prenons comme exemple la liaison glycosidique d'un diholoside glucosidique qui est définie par :
- la nature des 2 oses qui entrent dans sa composition,
- leur configuration D ou L (
projection de Fischer),
- leur forme cyclique (pyrane ou furane),
- leur configuration D ou L (
- le numéro du carbone anomérique, i.e. C1 pour les aldoses et C2 pour les cétoses et leur forme (α ou β),
- la configuration anomérique de la liaison glycosidique.
En outre, les termes suivants sont employés :
- ...ose, i.e. la fonction hémiacétalique de l’ose est libre, ose engagé par une fonction alcool ($\ce{R-OH}$), le numéro de l’atome de carbone portant la fonction alcool est indiqué,
- ...osyl/osido, i.e. la fonction hémiacétalique du premier ose est engagée dans la liaison glycosidique,
- ...oside, i.e. la fonction hémiacétalique du dernier ose est engagée dans la liaison glycosidique.
2. Nomenclature : D/L-nom de l'ose terminé par osyl ([α ou β][1 ou 2] n [carbone non anomérique]) D/L-nom de l'ose terminé par ose/oside.
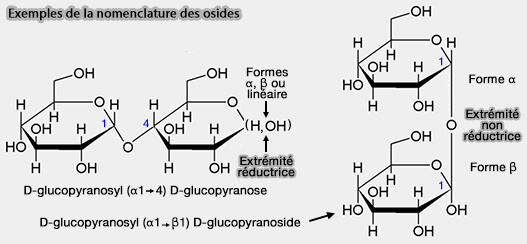
(Figure : vetopsy.fr)
Remarque : Les méthodes d'étude de la liaison glycosidique sont bien expliquées dans : Les osides.
Holosides
Oligosides (oligosaccharides)
1. Les oligosides (oligosaccharides par anglicisme) sont des oligomères formés d'un nombre n d'oses (ou monosaccharides) par liaison glycosidique (α ou β).
- Le nombre d'oses n varie entre 2 et 10, mais peut aller jusqu'à 25 selon les sources.
- Leur hydrolyse aboutit uniquement à des oses.
2. Les oligosides sont rarement libres et sont liés le plus souvent de façon covalente pour former des glycoconjugués.
- Avec les lipides, ils forment des glycolipides.
- Avec des protéines, ils forment les glycoprotéines.
Remarque : les glycolipides et les glycoprotéines membranaires sont localisés sur le feuilet externe des membranes.
| Oligosides (oligosaccharides) | ||||||
|---|---|---|---|---|---|---|
| Diholosides (disaccharides) | Triholosides (trisaccharides) |
|||||
| Réducteurs | Non réducteurs | |||||
| État libre | ||||||
| Lactose | Galactose Glucose β (14) |
Lait | Saccharose (sucrose en anglais) |
Glucose Fructose (α1β2) |
Végétaux |
Gentianose |
| Tréhalose | Glucose Glucose α(11) |
Champignons, bactéries, hémolymphe) |
Raffinose |
|||
| Hydrolyse des polyosides | ||||||
| Maltose et isomaltose |
Glucose Glucose β (14) |
Glycogène et amidon |
… | |||
| Cellobiose | Glucose Glucose β (14) |
Cellulose | … | |||
| Autres… | ||||||
Polyholosides ou polysaccharides
1. Les polyholosides (polysaccharides par anglicisme) sont constitués par l’enchaînement de quelques dizaines jusqu’à plusieurs milliers de résidus d’oses.
Ils ont deux fonctions principales.
- ils servent de réserve énergétique glucidique, i.e. glycogène, amidon, galactogène, inuline...
- ils structurent certaines cellules, i.e. chitine, cellulose...
2. Les polyosides sont appelés aussi glycanes :
- homopolysaccharides ou homoglycanes si tous ses monosaccharides sont du même type,
- hétéropolysaccharides ou hétéroglycanes lorsque plusieurs types de monosaccharides sont présents.
| Polyholosides (polysaccharides) | |||||
|---|---|---|---|---|---|
| Polyholosides homogènes (hydrolyse oses) |
Polyholosides hétérogènes (hydrolyse oses, acides uroniques, osamines, acides sialiques) |
||||
| Glucosanes | Autres hexosanes | ||||
| de réserve | de structure | ||||
| Glycogène | Animaux | Cellulose | Végétaux (certaines bactéries) |
Galactogène | Gommes |
| Amidon (amylose + amylopectine) |
Végétaux | Chitine | Squelette (invertébrés) |
Pectines | Agarose (agar-agar) |
| Inuline | Certains végétaux |
Arabinoxylanes | Polyuronides (acide glucuronique) |
||
| Dextranes | Bactéries Levures |
||||


