Voies métaboliques
Pyruvate et maladies neurodégénératives
Syndrome de Leigh et maladie de Parkinson
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

La perturbation du pyruvate dans les astrocytes explique une grande partie de la pathogénie des maladies neurodégénératives, en particulier la maladie de Parkinson et de Leight.
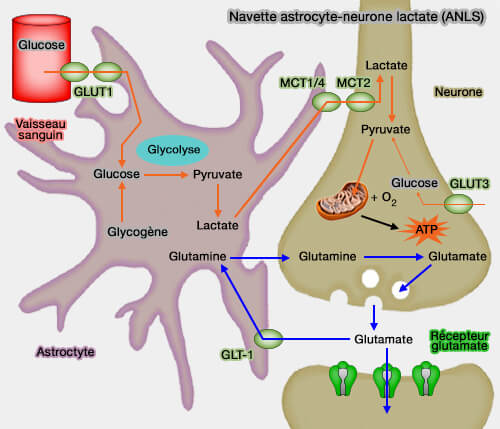
(Figure : vetopsy.fr)

La perturbation de toutes les fonctions des astrocytes dans les maladies neurodégénératives explique les symptômes observés (
Syndrome de Leigh
Le syndrome de Leigh est une affection dans laquelle près de la moitié des patients sont atteints d'un déficit en pyruvate déshydrogénase (PDH), enzyme qui convertit le pyruvate en acétyl-CoA :
$\ce{Pyruvate + CoA-SH + NAD+}$ $\ce{->}$ $\ce{NADH + H+ + CO2 + Acétyl-CoA}$
Cette maladie attaque principalement les ganglions de la base, le thalamus et le tronc cérébral (The Spectrum of Pyruvate Dehydrogenase Complex Deficiency: Clinical, Biochemical and Genetic Features in 371 Patients 2012).
- Elle perturbe la phosphorylation oxydative - OXPHOS - (OXPHOS mutations and neurodegeneration 2013).
- Les malades ont un déficit dans l'apprentissage de la marche, des réactions fortement diminuées aux stimuli sensoriels et donc, une difficulté à interagir avec leur environnement. Les malades décèdent, en général, avant 10 ans.
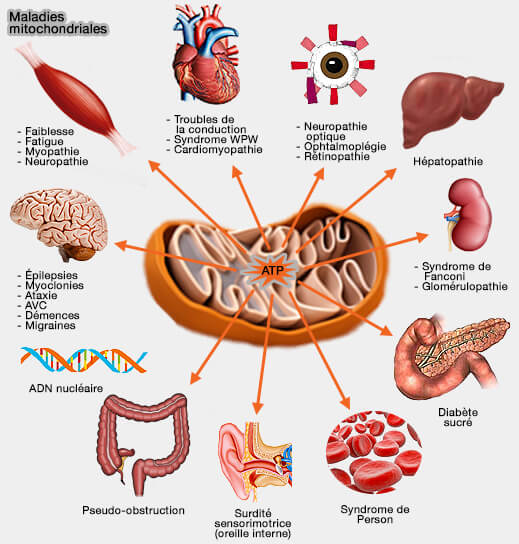
(Figure : vetopsy.fr d'après Goldstein)
Maladie de Parkinson
La maladie de Parkinson est la deuxième maladie neurodégénérative la plus fréquente après la maladie d'Alzheimer.
- La perte de ces neurones provoque d'importants dysfonctionnements neurologiques moteurs et non moteurs qui cractérisent l'évolution clinique de la maladie de Parkinson (Parkinson’s disease: clinical features and diagnosis 2009).
- Le dysfonctionnement mitochondrial est aussi essentiel à sa pathogénie (Mitochondrial dysfunction and oxidative stress in Parkinson’s disease and monogenic parkinsonism 2013 et The role of calcium and mitochondrial oxidant stress in the loss of substantia nigra pars compacta dopaminergic neurons in Parkinson’s disease 2012).
1. Les neurones dopaminergiques de la substantia nigra (substance noire ou locus niger) sont particulièrement sensibles aux dommages oxydatifs et sont détruits par la production de ROS et de RNS (dérivés réactifs de l'azote).

L'hypométabolisme serait un contributeur important dans l'évolution de la maladie.
2. Dans les neurones dopaminergiques de la substantia nigra de la maladie de Parkinson et des patients parkinsoniens subcliniques, de nombreux gènes diminueraient l'expression du métabolisme du pyruvate et de la chaîne respiratoire de transport d'électrons.
- Ces gènes sont sous le contrôle de PGC-1α (Peroxisome Proliferator-activated receptor Gamma Coactivator 1-alpha), un facteur de transcription responsable de la biogenèse mitochondriale et de la régulation, qui est sous-exprimée dans la maladie de Parkinson (PGC-1α, A Potential Therapeutic Target for Early Intervention in Parkinson’s Disease 2011).
- Chez le rat, la surexpression de PGC-1α supprime la perte de neurones dopaminergiques.
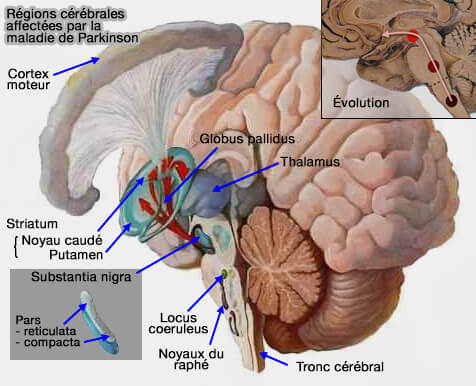
(Figure : vetopsy.fr d'après Lajoie et coll pour la fig. droite)
Cet hypométabolisme peut être vu sur l'imagerie TEP-FDG (Tomographie par Émission de Positons par le FluoroDésoxyGlucose) chez les patients atteints de la maladie de Parkinson, tout comme chez les patients atteints de la maladie d'Alzheimer, ce qui pourrait déboucher sur de nouveaux traitements (Pharmacological approaches to restore mitochondrial function 2013).
Nouvelles pistes thérapeutiques
1. La maladie d'Alzheimer et la maladie de Parkinson partagent de nombreuses similitudes :
- augmentation de la production de ROS,
- états hypométaboliques,
- dysfonctionnement métabolique global dans leurs régions respectives du cerveau.
a. Dans la maladie d'Alzheimer, deux thérapeutiques sont prescrites qui ne corrigent que peu le cogntion (Treatment of Alzheimer Disease 2011).
- Les inhibiteurs de l'acétylcholinestérase (AChEI) augmentent les niveaux corticaux d'acétylcholine, diminués dans cette maladie.
- Les inhibiteurs des récepteurs NMDA bloquent la liaison du glutamate au récepteur NMDA, empêchant la toxicité excitatrice neuronale.
b. Dans la maladie de Parkinson, les patients atteints sont généralement traités avec :
- de la L-Dopa, un précurseur de la dopamine,
- des inhibiteurs du catabolisme de la dopamine comme la tolcapone qui inhibe la catéchol-O-méthyltransfèrase (COMT).

Or, l'hypométabolisme du pyruvate et la surproduction de ROS, observés et dans la maladie d'Alzheimer et dans la maladie de Parkinson, ne sont pas traités et pourraient être corrigés par l'administration de pyruvate.
2. Le pyruvate protège contre les ROS (dérivés réactifs de l'oxygène) et les RNS (dérivés réactifs de l'azote).
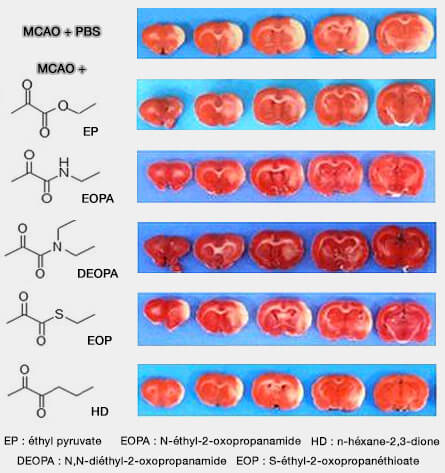
(Figure : vetopsy.fr d'après Lee et coll)
a. Dans les neurones de rat primaires cultivés, l'administration de pyruvate inhibe la mort neuronale oxydative induite par la bêta-amyloïde (Aβ).
- Dans un modèle murin de la maladie de Parkinson, l'administration d'éthyl pyruvate, un ester éthylique du pyruvate hydrolysé en pyruvate et éthanol, protège les neurones substantia nigra de la neurotoxicité oxydative (Ethyl Pyruvate Rescues Nigrostriatal Dopaminergic Neurons by Regulating Glial Activation in a Mouse Model of Parkinson’s Disease 2011).
- Dans la figure ci-contre, tirée de l'article Anti-inflammatory and anti-excitoxic effects of diethyl oxopropanamide, an ethyl pyruvate bioisoster, exert robust neuroprotective effects in the postischemic brain 2016, MCAO signifie rat middle cerebral artery occlusion qui provoque une lésion ischémique. La récupération est visible avec les dérivés de l'éthyl-pyruvate (PBS, tampon phosphate salin).
b. L'effet protecteur du pyruvate reposerait sur l'oxydation du pyruvate et la production importante de NADH, qui peut être converti en NADPH mitochondriale via la NADP-transhydrogénase : les concentrations de ROS sont abaissés par la reconstitution des taux de glutathion réduit (Cofactor Balance by Nicotinamide Nucleotide Transhydrogenase (NNT) Coordinates Reductive Carboxylation and Glucose Catabolism in the Tricarboxylic Acid (TCA) Cycle 2013).
2. Dans un modèle murin de la maladie d'Alzheimer, provoqué par une neutotoxine, le MPTP (1-méthyl-4-phényl-1,2,3,6-tétrahydropyridine), l'administration de pyruvate et du corps cétonique β-D-hydroxybutyrate directement dans le liquide céphalo-rachidien corrige la neurotoxicité excitatrice et de la déficience énergétique neuronale (Dietary energy substrates reverse early neuronal hyperactivity in a mouse model of Alzheimer's disease 2013).

Le pyruvate et le 3-bêta-hydroxybutyrate fourniraient une source d'énergie sans glucose qui permettait d'éviter l'utilisation du glycogène astrocytaire, et permettait de maintenir l'homéostasie synaptique.


