Lipides
Acides gras : catabolisme des acides gras
Cétogenèse
et corps cétoniques
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Composés organiques
- Protides
- Acides nucléiques
- Glucides
- Lipides
- Vue d'ensemble des lipides
- acides gras (FA)
- Classification des lipides
- Cholestérol
- Glycérides
- Trafic non vésiculaire des lipides et LTP
- Digestion et absorption entérocytaire des lipides
- Lipoprotéines
- Gouttelettes lipidiques (LD)
- Coenzymes
- Hormones
- Composés inorganiques
- Composés organiques
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

L'acétyl-CoA produit par la bêta-oxydation (β-oxydation ou FAO, fatty Acid β-Oxydation) peut, outre rentrer dans le cycle de Krebs, former des corps cétoniques par la cétogenèse dans les hépatocytes.
Vue d'ensemble de la cétogenèse
1. Lorsque l'organisme ne peut utiliser les réserves de glucose, la cétogenèse est déclenchée et engendre la formation de :
- l'acétylacétate,
- le β-D-hydroxybutyrate (BHB),
- l'acétone.

La cétogenèse a lieu dans les hépatocytes et les corps cétoniques constituent une source d’énergie supplémentaire utilisée par tous les tissus, y compris le cerveau.
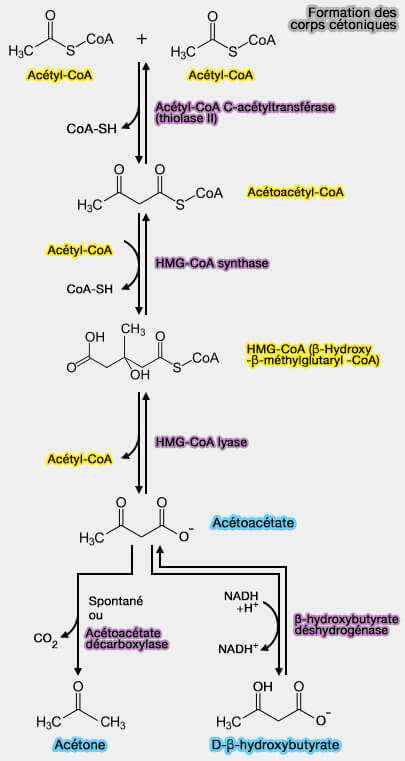
(Figure : vetopsy.fr)
2. Toutefois, certains tissus, i.e. muscle, coeur, rein, cerveau, utilisent préférentiellement les corps cétoniques même si le glucose est parfaitement disponible.
Par exemple, le β-hydroxybutyrate et l'acétoacétate peuvent facilement traverser les membranes et constituent donc une source d'énergie pour le cerveau, qui ne peut pas métaboliser directement les acides gras.
- Le cerveau reçoit 60 à 70 % de l’énergie dont il a besoin des corps cétoniques lorsque la glycémie est basse.
- Ces corps sont transportés dans le cerveau par des transporteurs SLC, i.e. de la famille des transporteurs de monocarboxylates (MCT ou SLC16), i.e. MCT1 (SLC16A1) et MCT2 (SLC16A7).

Vous pouvez lire : Multi-dimensional roles of ketone bodies in fuel metabolism, signaling, and therapeutics (2017).
Synthèse des corps cétoniques
Acétoacétyl-CoA
Formation de l'acétoacétyl-CoA
1. Dans les hépatocytes, deux molécules d'acétyl-CoA peuvent se combiner pour former l'acétoacétyl-CoA, réaction catalysée par l'acétyl-CoA C-acétyltransférase ou thiolase II (EC 2.3.1.9), une β-cétothiolase.
$\ce{2 Acétyl-CoA}$ $\leftrightharpoons$ $\ce{Acétoacétyl-CoA + CoA}$
Remarque : la thiolase I ou 3-cétoacyl-CoA thiolase joue un rôle dans la 4ème étape de la β-oxydation.
2. On trouve deux isoformes appelées malheureusement ACAT, comme l'enzyme d'estérification du cholestérol, l'acyl cholestérol acyltransférase qui n'est pas la même enzyme, i.e. EC 2.3.1.26. :
- ACAT1 est l'isoforme mitochondriale, appelée aussi acétoacétyl-CoA thiolase,
- ACAT2 et est l'isoforme cytosolique, appelée aussi acétoacétyl-CoA thiolase cytosolique.
3. L'acétoacétyl-CoA peut être aussi produit par β-oxydation duc.
Devenirs de l'acétoacétyl-CoA
Dans le foie
1. L'acétoacétyl-CoA peut donner naissance à l'HMG-CoA ou 3-Hydroxy-3-méthylglutaryl-CoA, réaction catalysée par la HMG-CoA synthase ou Hydroxyméthylglutaryl-CoA synthase (HMGCS2), i.e.EC 2.3.3.10.
$\ce{Acétoacétyl-CoA + acétyl-CoA}$ $\leftrightharpoons$ $\ce{HMG-CoA + CoA}$
a. Cette synthèse peut s'effectuer également grâce à deux isoformes :
- soit dans le cytosol, grâce à l'isoforme soluble HMGCS1 pour la synthèse du cholestérol par la voie dite du mévalonate,
- soit dans les mitochondries, grâce à HMGCS2 pour la suite de la cétogenèse.
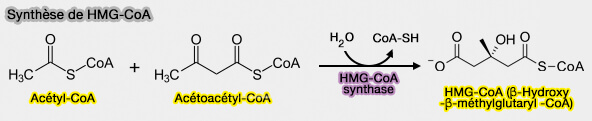
(Figure : vetopsy.fr)
b. HMG-CoA synthase est une enzyme limitante clé dans la cétogenèse par l'activation de son et l'activation de la protéine HMGCS2 (Molecular Mechanisms for Ketone Body Metabolism, Signaling Functions, and Therapeutic Potential in Cancer 2022).
2. La HMG-CoA peut suivre plusieurs voies.
a. Dans les mitochondries, a HMG-CoA lyase ou 3-hydroxy-3-méthylglutaryl-CoA lyase (HMGCL), i.e. EC 4.1.3.4, une désacylase hépatique, peut produire de l'acide acétylacétique (ou acetoacetic en anglais) selon la réaction :
$\ce{HMG-CoA}$ $\leftrightharpoons$ $\ce{Acétoacétate + acétyl-CoA}$
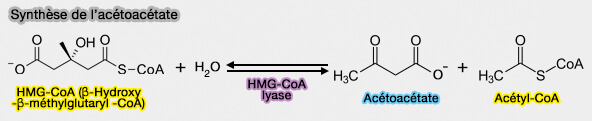
(Figure : vetopsy.fr)
b. Dans la fraction microsomale du réticulum endoplasmique (RE), sous l'nfluence de la HMGCR (3-hydroxy-3-méthylglutaryl-CoA réductase), enzyme à NADPH ou NADH, elle conduit au mévalonate et à la synthèse de novo du cholestérol et des stéroïdes.
3. L'acétoacétate peut être métabolisé pour former les deux autres corps cétoniques.
- Il est réduit en β-D-hydroxybutyrate (BHB), réaction réversible,
- Il est décarboxylé en acétone, la plus simple des cétones.
4. Il peut aussi passer directement dans le sang par la famille des transporteurs de monocarboxylates (MCT ou SLC16) pour rejoindre les tissus périphériques.
Dans les tissus périphériques : cétolyse
1. Dans les tissus périphériques (extra-hépatiques), la 3-oxoacid CoA-transférase (SCOT), i.e. EC 2.8.3.5, une thiophorase absente du foie, peut catalyser faiblement la réaction :
$\ce{Acétoacétyl-CoA + succinate}$ $\leftrightharpoons$ $\ce{Acide acétylacétique + succinyl-CoA}$
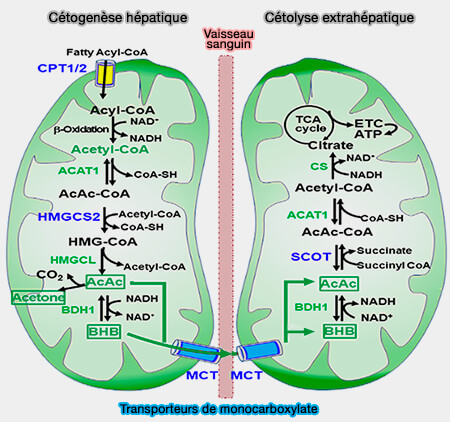
(Figure : vetopsy.fr d'après Hwang et coll)
2. Toutefois, dans les conditions normales, la réaction est en sens inverse et retransforme l'acide acétoacétique en acétoacétyl-CoA pour amorcer la cétolyse (Molecular Mechanisms for Ketone Body Metabolism, Signaling Functions, and Therapeutic Potential in Cancer 2022).
L'acétoacétyl-CoA obtenu est transformé en acétyl-CoA par l'ACAT1, qui va se condenser avec l'oxaloacétate pour former le citrate qui entre dans le cycle de Krebs.
3. SCOT est une enzyme limitante dans la cétolyse par l'activation de son et l'activation de sa protéine (Molecular Mechanisms for Ketone Body Metabolism, Signaling Functions, and Therapeutic Potential in Cancer 2022).

Comme le foie ne produit pas de SCOT, il synthétise, mais utilise peu les corps cétoniques.
β-D-hydroxybutyrate (BHB)
1. Le β-D-hydroxybutyrate (BHB) le plus abondant des corps cétoniques, est obtenu par plusieurs voies.
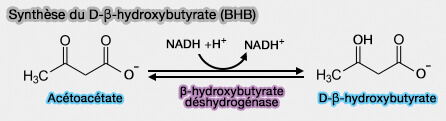
(Figure : vetopsy.fr)
a. via l'acétoacétate, réaction catalysée par la β-hydroxybutyrate déshydrogénase (BH1), i.e. EC 1.1.1.30, enzyme à NADH.
$\ce{Acétoacétate + NADH+ + H+}$ $\leftrightharpoons$ $\ce{β-D-hydroxybutate + NAD+}$
b. par le métabolisme de l'acide butyrique par une série de réaction :
Butyrate →
Butyryl-CoA
→
Crotonyl-CoA
→
β-hydroxybutyryl-CoA
→
Poly-β-hydroxybutyrate
→ D-β-(D-β-hydroxybutyryloxy)-butyrate → D-β-hydroxybutyrate
2. Le butyryl-CoA peut aussi être un intermediaire dans la β-oxydation.
Remarque : l'acide β-Hydroxy β-méthylbutyrique (HMB) est employé comme complément alimentaire dans la cicatrisation des plaies et dans les atrophies musculaires dues au cancer ou au SIDA.
Acétone
1. L'acétone est produite par la décarboxylation de l'acide acétoacétique, réaction spontanée chez l'homme ou catalysée par l'acétoacétate décarboxylase (AAD), i.e. EC 4.1.1.4.
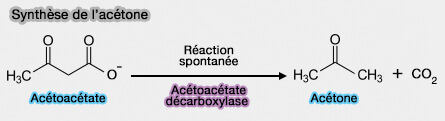
(Figure : vetopsy.fr)
La présence de cette enzyme est encore controversée car elle a été retrouvée dans le sérum humain, mais pas dans les tissus.
2. L'acétone peut être utilisée par les tissus par la suite.
a. Elle peut former de l'hydroxyacétone (acétol) grâce à CYP2E1 et ensuite via le propylène glycol (propane-1,2-diol) transformé en :
- acétate, qui peut être convertit en acétyl-CoA,
- acide méthanoïque ou formique CHOOH, qui peut enter dans le pool des méthyles.
b. Elle peut aussi former du méthylglyoxal (pyruvaldéhyde ou 2-oxopropanal) ou MG, métabolite non seulement des lipides, mais aussi des protéines et des glucides (Methylglyoxal and Its Adducts: Induction, Repair, and Association with Disease 2022).
- Le MG peut modifier de manière covalente l'ADN, l'ARN et les protéines, formant des produits finaux de glycation avancée (MG-AGE).
- Les MG et les MG-AGE sont associés à l’apparition et à la progression de nombreuses pathologies, notamment le diabète, le cancer et les maladies hépatiques et rénales.
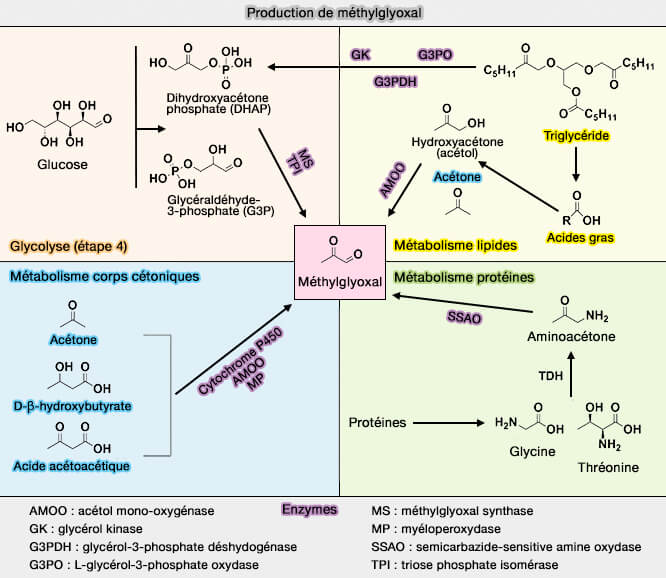
(Figure : vetopsy.fr d'après Lai et coll)
Régulation et fonctions des corps cétoniques
BiochimieChimie organiqueBioénergétiqueProtidesGlucidesLipidesacides gras (FA)Synthèse des acides grasβ-oxydationCorps cétoniquesOxylipinesLipides vraisLipides vrais simplesLipides vrais complexesLipoïdesCholestérolGlycéridesPhospholipidesGlycérophospholipidesSphingophospholipidesTrafic non vésiculaire et LTPDigestion et absorption entérocytaire des lipidesLipoprotéinesApolipoprotéinesGouttelettes lipidiques (LD)EnzymesCoenzymesVitaminesHormonesComposés inorganiquesTransport membranaireMoteurs moléculairesVoies de signalisation


