Cycle cellulaire
Cyclin-Dependent Kinases (CDK)
Vue d'ensemble
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Les kinases dépendantes des cyclines (CDK) constituent un ensemble de protéines sérine/thréonine kinases hautement conservées qui jouent un rôle central dans le contrôle du cycle cellulaire, la régulation transcriptionnelle, la différenciation cellulaire et l’intégrité génomique.
Vue d'ensemble des CDK
Les CDK (Cyclin-Dependent Kinase) ou kinases dépendantes des cyclines constituent une famille de kinases sérine/thréonine hautement conservées chez les eucaryotes, essentielles à l’organisation temporelle du cycle cellulaire.
- L’activité des CDK dépend strictement de leur association avec une cycline (
interactions cycline/CDK)
- En l’absence de cycline, les CDK sont catalytiquement inactives.

Les cyclines et les interactions cycline/CDK sont étudiées dans des chapitres spécifiques.
1. Les complexes cycline/CDK assurent la progression ordonnée du cycle cellulaire en contrôlant les grandes transitions :
- engagement en phase G1,
- initiation de la réplication en phase S,
- préparation de l’entrée en mitose en phase G2,
- déclenchement et coordination de la mitose.
Cette fonction repose sur la phosphorylation ciblée de nombreux substrats impliqués dans :
- la structure de la chromatine, phosphorylationdes histones, notamment H1 et H3 (Ser 10) et des condensines (kleisines CAP-D2, CAP-H),
- la réplication de l’ADN, phosphorylation du complexe de pré‑réplicatif (pré-RC) avec Cdc6 et MCM2-7, Treslin et TopBP1,
- l’organisation du fuseau mitotique, phosphorylation de kinésines (Eg5/KIF11), des MAP (Microtubule-Associated Proteins) comme NuMA et TACC3,
- la dynamique nucléaire, i.e. rupture de l’enveloppe nucléaire par phosphorylation des lamines A/C et de Nup98, et cytosquelettique, microtubules et actine (cortex nucléaire) par phosphorylation de MAP (MAP4, Stathmine) et de myosine II (MLC)
2. Les CDK ne fonctionnent pas comme des enzymes autonomes, mais comme des intégrateurs d’un réseau de signaux régulatoires.
a. Leur activité est intégrée dans un réseau de régulation qui inclut :
- la disponibilité des cyclines, complexes cycline D/CDK4-6 en G1, complexe cycline E/CDK2 à la ttransition G1/S,
- les mécanismes de phosphorylation et de déphosphorylation, activation par CAK (cycline H/CDK7/Mat1) et inhibition par Wee1 contrebalancée par Cdc25A,
- les CKI (CDK inhibitors), les checkpoints, p21CIP1, p27KIP1, p16INK4a sous contrôle des voies ATR/Chk1 et ATM/Chk2,
- les systèmes de dégradation protéique, ubiquitination des cyclines par SCFFbxw7 et APC/CCdc20/APC/CCdh1,
b. Certaines CDK possèdent également des fonctions en dehors du cycle cellulaire et participent notamment à :
- la régulation de la transcription, CDK7 (TFIIH) et CDK9 (P-TEFb) phosphorylant le CTD de l’ARN polymérase II,
- la réponse aux dommages de l’ADN, CDK2 phosphorylant RBBP8 (CtIP) pour contrôler la résection des cassures double brin,
- la différenciation cellulaire, CDK5 dans la différenciation et la migration neuronales,
- l’organisation de programmes cellulaires spécialisés, CDK8 comme module régulateur du complexe Mediator dans les programmes transcriptionnels contextuels.

Ainsi, les CDK constituent le noyau catalytique du contrôle du cycle, mais leur activité reflète toujours l’état global de la cellule.
Structure et activation
Les CDK présentent une structure globale conservée typique des kinases sérine/thréonine, adaptée à une régulation stricte de leur activité, mais présentent des particularités structurales responsables de leur dépendance aux cyclines.
1. Chaque CDK possède un domaine catalytique bilobé.
a. Le lobe N-terminal, riche en feuillets β, contient :
- la glycine-rich loop (GxGxxGxV), boucle flexible impliquée dans l’ancrage et l’orientation de l’ATP au sein du site catalytique,
- l’hélice αC, élément clé de l’activation conformationnelle.
b. Le lobe C-terminal, majoritairement α-hélicoïdal :
- contient les sites de reconnaissance des substrats, impliquant aussi des surfaces créées à l’interface CDK–cycline,
- porte plusieurs motifs catalytiques hautement conservés,
- inclut des hélices structurales secondaires (dont l’hélice αL12) qui contribuent à la stabilité architecturale du lobe C-terminal et peuvent moduler indirectement sa dynamique conformationnelle,
- inclut également l’hélice αE, impliquée dans le couplage allostérique entre la fixation de la cycline, l’organisation de la boucle T et la stabilisation du site catalytique.
Le site catalytique se situe dans la fente entre les deux lobes.
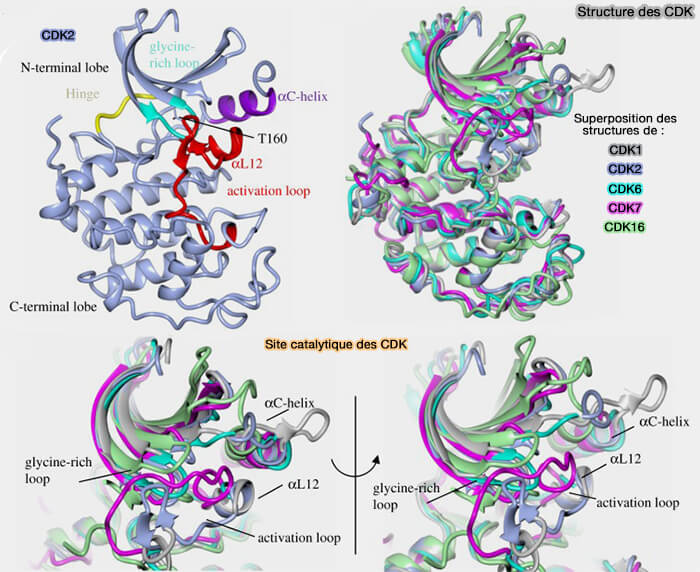
(Figure : vetopsy.fr d'après Wood et Endicott)
2. Comme toutes les kinases, les CDK possèdent plusieurs motifs structuraux essentiels à la catalyse, mais dont l’organisation spatiale est incompatible avec une activité efficace en absence de cycline.
- Le motif VAIK contient la lysine catalytique qui participe participe à l’ancrage de l’ATP.
- Le motif HRD dans la boucle catalytique est essentiel au transfert du groupement phosphate.
- Le motif DFG, au début de la boucle d’activation, contrôle l’orientation catalytique du site actif.
3. La boucle T (T-loop ou activation loop) est un élément central du contrôle structural des CDK.
- En absence de cycline, cette boucle adopte une conformation qui obstrue partiellement le site catalytique, rendant l’enzyme inactive.
- La fixation d’une cycline induit un réarrangement conformationnel qui expose la boucle T et prépare la CDK à son activation complète (
interactions CDK/cycline).
- La phosphorylation d’un résidu conservé de la boucle T (Thr160 sur CDK2, Thr161 sur CDK1) stabilise la conformation active (
activation par la CAK).
4. La poche de liaison à l’ATP est une structure composite formée par :
- la glycine-rich loop, qui coiffe l’ATP,
- la lysine catalytique du motif VAIK, qui coordonne les phosphates,
- l’hélice αC, via le glutamate conservé qui forme un pont ionique avec la lysine,
- des résidus du lobe C-terminal qui complètent la fente catalytique.
5. La plupart des CDK possèdent un motif conservé dans l’hélice αC, classiquement désigné par le motif PSTAIRE (ou variantes proches selon la CDK) qui constitue une interface essentielle pour l’interaction avec la cycline.
La liaison de la cycline à cette interface provoque une réorganisation de l’hélice αC, contribuant à l’alignement correct des résidus catalytiques et à l’activation fonctionnelle de la kinase.
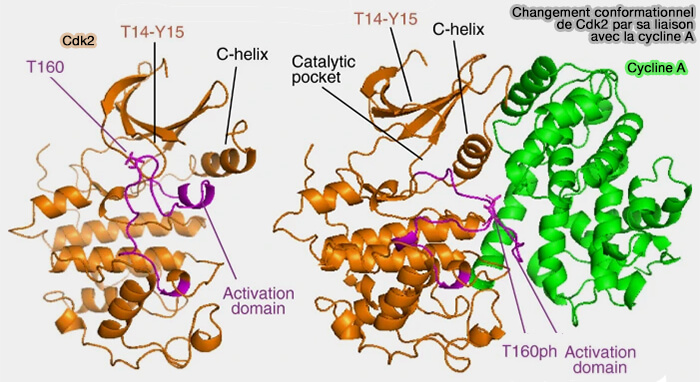
(Figure : vetopsy.fr d'après Malumbres)
5. Les CDK existent donc sous plusieurs états structuraux, exemple classique de régulation enzymatique par allostérie structurale, i.e. changement de conformation induit par la fixation d’un partenaire sur un site distinct du site actif.
- Une CDK libre adopte une conformation inactive, caractérisée par une hélice αC désalignée et une T-loop qui obstrue partiellement le site catalytique.
- Une CDK liée à une cycline subit un réarrangement conformationnel global qui rend le site catalytique partiellement fonctionnel.
- Une CDK associée à une cycline et phosphorylée sur la T-loop adopte une conformation pleinement active, compatible avec une catalyse efficace.
Principe général d’activation des CDK
L’état actif d’une CDK reflète un équilibre dynamique entre :
- disponibilité de la cycline partenaire, cycline D/CDK4-6 en G1, cycline E/CDK2 à la transition G1/S, cycline B/CDK1 (MPF) en entrée de mitose,
- phosphorylation d’activation,
- phosphorylations inhibitrices,
- présence ou absence de CKI (CDK inhibitors).
Ce principe explique pourquoi les CDK ne fonctionnent jamais comme de simples enzymes constitutives, mais comme des intégrateurs moléculaires de l’état cellulaire.
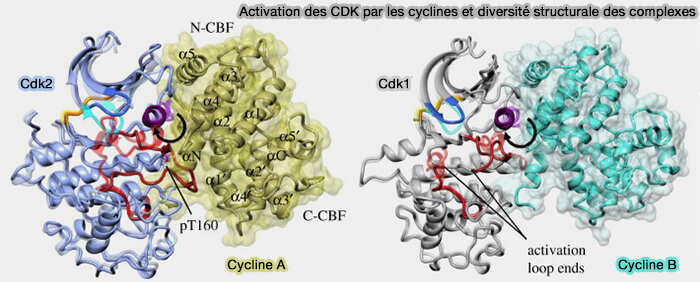
(Figure : vetopsy.fr d'après Wood et Endicott)
1. L’activation complète de la CDK nécessite la phosphorylation d’un résidu conservé de la boucle T (Thr160 pour CDK2, Thr161 pour CDK1).
- Cette phosphorylation est assurée par la kinase d’activation des CDK (CAK), complexe cycline H/CDK7,
- Elle stabilise la conformation active de l’enzyme et augmente fortement son efficacité catalytique.

L'activation des CDK est étudiée dans un chapitre spécifique.
2. À l’inverse, certaines phosphorylations maintiennent les CDK dans un état inactif.
- Les kinases Wee1 et Myt1 (PKMYT1) phosphorylent CDK1 et CDK2 sur des résidus inhibiteurs (Thr14 et Tyr15), ce qui empêche l’entrée prématurée en phase M ou en phase S.
- La levée de cette inhibition dépend de l’activité des phosphatases Cdc25.
3. Les inhibiteurs spécifiques appelés CKI (CDK inhibitors) peuvent également bloquer l'activation des CDK.
- Les protéines de la famille CIP/KIP, p21, p27 et p57, sous contrôle des voies ATR/Chk1 et ATM/Chk2, inhibent plusieurs complexes cycline/CDK.
- Celles de la famille INK4, p16, p15, p18 et p19, ciblent préférentiellement CDK4 et CDK6.

L'inhibition des CDK est étudiée dans des chapitres spécifiques.
Logique fonctionnelle des complexes cycline/CDK
L’activité des complexes cycline/CDK suit une logique dynamique fondée sur des seuils d’activité plutôt que sur un simple mode binaire actif/inactif.
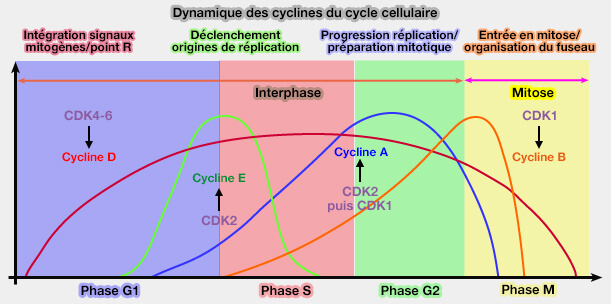
(Figure : vetopsy.fr)
1. Chaque phase du cycle cellulaire correspond à un niveau caractéristique d’activité CDK.
- Une activité faible est compatible avec la préparation de la réplication en phase G1
- Une activité intermédiaire permet l’engagement en phase S.
- Un niveau élevé d’activité est requis pour l’entrée en mitose.
Cette organisation explique que certaines transitions sont :
2. Cette organisation par seuils et transitions garantit que les événements majeurs du cycle ne se chevauchent pas de manière anarchique, mais s’enchaînent selon une logique cohérente et robuste.

Les complexes cycline/CDK sont étudiés dans les chapitres spécifiques de leurs cyclines.
Diversité fonctionnelle des CDK
Les CDK forment une famille homogène sur le plan structural, mais diversifiée sur le plan fonctionnel selon leur contexte d’expression et leurs partenaires, ce que synthétise le tableau suivant.
| CDK | Fonction générale | Contexte d’expression dominant |
Remarque clé |
|---|---|---|---|
| CDK du cycle cellulaire | |||
| CDK1 |
|
Cellules prolifératives |
Essentielle à la division, peut compenser CDK2/4/6 dans de nombreux contextes |
| CDK2 | Contrôle entrée en phase S |
Cellules prolifératives |
Redondance partielle avec CDK1 |
| CDK3 |
|
Cellules prolifératives |
|
| CDK4 | Engagement en G1 |
Cellules prolifératives |
Cible majeure des CKI INK4 |
| CDK6 |
|
Cellules hématopoïétiques notamment |
Rôle hors cycle dans certaines différenciations |
| CDK impliquées dans la transcription | |||
| CDK7 |
|
Expression ubiquitaire |
|
| CDK8 | Modulation transcriptionnelle |
Expression ubiquitaire |
Sous-unité du Mediator |
| CDK9 | Élongation transcriptionnelle |
Expression ubiquitaire |
Complexe P-TEFb |
| CDK12 | Régulation gènes DDR |
Expression ubiquitaire |
Rôle majeur dans réponse aux dommages de l’ADN |
| CDK13 | Régulation ARN pol II |
Expression ubiquitaire |
Fonctions proches de CDK12 |
| CDK spécialisées / contextuelles | |||
| CDK5 |
|
Neurones |
|
| CDK10 |
|
Faiblement exprimée |
Fonctions encore mal caractérisées |
| CDK11 |
|
Expression ubiquitaire |
Isoformes multiples (CDK11A/B) |
| CDK14 |
|
Expression tissulaire variable |
Interaction avec cycline Y |
| CDK15 |
|
Faiblement exprimée |
Fonctions encore peu caractérisées |
| CDK16 |
|
|
Activée par cycline Y |
| CDK17 | Organisation cellulaire | Tissus différenciés |
Activée par cycline Y |
| CDK18 |
|
Expression faible |
|
Les CDK constituent un module enzymatique conservé dont la fonction dépend largement de leur contexte d’activation et de leurs partenaires, ce qui explique leur diversité fonctionnelle au sein de la cellule.
Régulation des CDK
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


