Cycle cellulaire
Reproduction cellulaire
Principaux points de contrôle
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Les points de contrôle du cycle cellulaire ou checkpoints coordonnent l’arrêt, la reprise ou l’abandon du cycle cellulaire en fonction de l’intégrité du génome, de l’état de la réplication et de la qualité de la ségrégation chromosomique.
1. Les points de contrôle du cycle cellulaire, ou checkpoints, correspondent aux principaux dispositifs intégrés qui vérifient, à différentes étapes, que les conditions intracellulaires permettent la poursuite du cycle.
- Chaque point de contrôle constitue un point d’arrêt potentiel du cycle cellulaire, au cours duquel l’état fonctionnel de la cellule est évalué.
- La progression à travers les différentes phases du cycle cellulaire ne se produit que lorsque ces conditions sont réunies.
Les points de contrôle sont :
- le checkpoint G1/S, qui contrôle l’intégrité de l’ADN avant l’engagement dans la réplication,
- le checkpoint de la phase S, qui surveille la progression des fourches de réplication,
- le checkpoint G2, qui vérifie l’achèvement de la réplication et la résolution des dommages résiduels,
- le checkpoint G2/M, qui conditionne l’entrée effective en mitose en autorisant l’activation du complexe cycline B/CDK1 (MPF),
- le point de contrôle du fuseau (SAC ou Spindle Assembly Checkpoint), assuré par le complexe MCC (Mitotic Checkpoint Complex), qui garantit la transition correcte de la métaphase vers l’anaphase.
2. La dynamique des checkpoints repose en grande partie sur le contrôle de l’activité des complexes cycline/CDK dont les différentes isoformes régulent spécifiquement chaque phase du cycle cellulaire.
Checkpoint G1/S
Le checkpoint G1/S est un mécanisme de surveillance qui empêche l’entrée en phase S lorsque l’intégrité du génome ou l’état cellulaire ne permettent pas une réplication fidèle de l’ADN.
Il agit en aval du point de restriction (R) de la phase G1, non pas comme un système décisionnel dépendant des signaux mitogènes, mais comme un verrou de sécurité fondé sur la détection active d’anomalies.
1. Le checkpoint G1/S repose sur une logique de protection du génome et vise principalement à empêcher la réplication d’un ADN endommagé, incomplètement réparé ou structurellement instable.
a. La détection des dommages repose sur les kinases ATR/Chk1 et ATM/Chk2 (
b. Toutefois, dans le contexte du checkpoint G1/S, leur signalisation converge principalement vers l’axe p53-p21CIP1, qui constitue le mécanisme effecteur spécifique du blocage en G1.
p53 induit alors l’expression du CKI (CDK inhibitors) p21CIP (CDKN1A), qui inhibe le complexe cycline E/CDK2, bloque l’hyperphosphorylation de Rb et maintient E2F sous forme inactive.

La cellule reste ainsi bloquée en G1, même si le point R a déjà été franchi.
Le checkpoint G1/S ne décide pas si la cellule doit proliférer, mais si elle est autorisée à répliquer son ADN en remplissant trois fonctions majeures :
- empêcher la réplication d’un génome endommagé,
- donner du temps aux mécanismes de réparation,
- orienter la cellule vers sénescence ou apoptose en cas de dommages irréparables.
Checkpoint S
La phase S comporte des mécanismes de surveillance stricts qui garantissent la fidélité de la réplication de l’ADN et la préparation de la cellule à la phase G2.
Toute anomalie ou dommage de l’ADN doit être détecté par le checkpoint S.
Activation du signal ATR-Chk1 et inhibition de CDK2
1. Les protéines ATR (Ataxia Telangiectasia and Rad3 related) et Chk1 (Checkpoint kinase 1) sont des sérine/thréonine kinases impliquées dans la détection de l’accumulation d’ADN simple brin (ssDNA) dans plusieurs contextes (Human single-stranded DNA binding proteins are essential for maintaining genomic stability 2013).
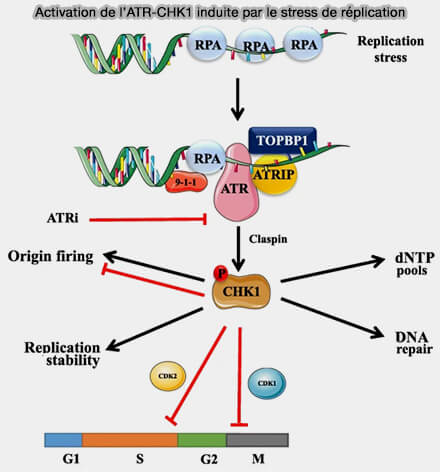
(Figure : vetopsy.fr d'après Mei et coll)
a. Dans les fourches de réplication bloquées, i.e. lorsque l’ADN polymérase est arrêtée ou ralentie, l’ADN simple brin (ssDNA) s’accumule et, recouvert de la protéine RPA (Replication Protein A), recrute ATR via son partenaire ATRIP (Ataxia telangiectasia and Rad3-related inhibitors and cancer therapy: where we stand 2019).
b. L'accumulation de stress de réplication survient lors de :
- manque de nucléotides,
- lésions de l’ADN,
- structures d’ADN difficiles à répliquer (zones riches en GC fortement condensées, hétérochromatine),
- collisions entre complexes de réplication et complexes de transcription,
- surexpression ou défaillance des protéines de réplication (hélicase, primase, ADN polymérase).
2. Dans ces circonstances, ATR empêche l’activation prématurée de CDK2 et de CDK1 (Fonctions et régulations de la kinase CHK1 dans l’hématopoïèse normale et leucémique 2019) :
a. en phosphorylant Chk1, qui inhibe secondairement l’activité des CDK en ciblant notamment :
b. en renforçant l’action de Wee1, non pas par phosphorylation directe, mais en inhibant Cdc25, en stabilisant Wee1 pendant le stress de réplication et en empêchant son inhibition par Plk1, ce qui maintient CDK1 phosphorylée sur Thr14/Tyr15 et donc inactive.
Ainsi, même si la cycline A est présente, CDK2 reste inactive tant que le stress de réplication ou les dommages persistent.
Remarque : ATM/Chk2 constitue une voie complémentaire activée principalement lorsque des cassures double brin (DSB) apparaissent.

L’activation de ces protéines entraîne un ralentissement ou un arrêt transitoire de la progression des fourches de réplication, permettant la réparation des anomalies avant leur transmission aux cellules filles.
Réponse globale du checkpoint S
1. D’une part, en réponse à l’activation du checkpoint S, les mécanismes de réparation de l'ADN sont activés.
a. En réponse à des dommages détectés, la cellule active :
- la réparation par excision de bases (BER),
- la réparation par excision de nucléotides (NER),
- la réparation des cassures double-brin par recombinaison homologue (HR) ou par jonction d’extrémités non homologues (NHEJ).
b. Ces mécanismes sont coordonnés pour préserver l’intégrité du génome.
2. D’autre part, le checkpoint S assure la prévention stricte du re-licensing des origines, afin de garantir que chaque segment du génome ne soit répliqué qu’une seule fois par cycle.
a. Ce contrôle repose sur plusieurs mécanismes complémentaires qui rendent les origines activées réfractaires à tout nouveau chargement du pré-RC pendant la phase S et la phase G2 :
- l’inhibition fonctionnelle de Cdt1 par la protéine géminine, qui empêche le rechargement du complexe MCM sur l’ADN,
- la dégradation de Cdt1 et de Cdc6 par ubiquitination dépendante de ligases E3 activées pendant la phase S, notamment CRL4Cdt2 et SCFSKP2,
- l’activité du complexe cycline A/CDK2, qui phosphorylent plusieurs licensing factors (ORC, Cdc6, Cdt1, MCM, géminine) et renforcent l’état réfractaire des origines.
b. Ces mécanismes coopèrent avec le signal ATR/Chk1 pour empêcher toute réinitiation aberrante de la réplication et préserver l’unicité de la duplication du génome.

À la fin de la phase S, une fois la réplication de l’ADN achevée, la cellule signale au checkpoint G2 que le génome est prêt pour la vérification finale.
- Si des erreurs persistent, la progression vers G2 est retardée jusqu’à réparation complète.
- Si les dommages sont irréparables, la cellule peut activer l’apoptose afin d’éviter la propagation de mutations.
Checkpoint G2
Le checkpoint G2 vérifie que la réplication du génome est complète et que l’ADN ne présente aucune anomalie avant l’engagement en mitose.
1. Le checkpoint G2 s’active à la fin de la phase S et fonctionne durant toute la phase G2.
Son objectif principal est que la cellule ne progresse vers la mitose que si :
- la réplication est entièrement achevée et toutes les fourches ont été résolues,
- aucune cassure double brin n’est détectée et aucune région n’est laissée non répliquée,
- les chromosomes sont structurellement intacts, i.e. leur organisation est validée.
2. Si des segments d’ADN simple brin persistent ou si le stress de réplication n’est pas totalement résolu, le signal ATR/Chk1 reste actif.
Cette activité maintient CDK1 inhibée, bloquant l’engagement en mitose tant que l’intégrité du génome n’est pas confirmée.
3. Le checkpoint G2 fonctionne ainsi comme un verrou final, garantissant que la cellule ne s’engage en mitose qu’une fois son génome stabilisé.
Checkpoint G2/M
Décision d'entrée en mitose
1. Le point de contrôle G2/M est un module décisionnel situé à la frontière entre la phase G2 et la mitose.
a. Le checkpoint G2/M détermine si la cellule peut activer le complexe cycline B/CDK1 (MPF), véritable déclencheur de l’entrée en mitose, en vérifiant que :
- la réplication est complète,
- l’ADN est intact,
- les lésions ont été réparées,
- aucun segment ne reste sous forme d’ADN simple brin ou non répliqué.
b. Il conditionne ainsi l’activation effective du MPF et l’entrée en prophase.
2. Lorsque la cellule a franchi tous les contrôles de la phase G2, Cdc25C déphosphoryle les sites inhibiteurs Thr14 et Tyr15 de CDK1, activant le MPF.
a. Une boucle de rétrocontrôle positif s’établit car le MPF activé phosphoryle directement :
- Cdc25C sur plusieurs résidus activateurs, ce qui augmente fortement son activité catalytique et entraîne la déphosphorylation de davantage de CDK1, libérant ainsi plus de complexes MPF actifs,
- Wee1, supprimant la kinase responsable de l’inhibition de CDK1.
b. Cette boucle de rétrocontrôle positif garantit une transition brutale, irréversible et synchronisée vers la mitose, comparable à un commutateur moléculaire.
| Résidu phosphorylé (Cdc25C) | Kinase responsable | Moment / Contexte | Conséquence fonctionnelle |
|---|---|---|---|
| Ser216 | Chk1/Chk2 | Dommages à l'ADN (checkpoint G2) |
Inhibition de Cdc25C par fixation de 14-3-3 ➞ Séquestration cytoplasmique, empêche l'entrée en mitose. |
| Ser214 | CDK1 (MPF) | Entrée en mitose |
Activation de Cdc25C ➞ renforce la déphosphorylation de CDK1 (boucle de rétroactivation positive). |
| Ser287 | PKA (ou autres kinases inhibitrices) |
Phase G2 | Maintien de Cdc25C inactive via interaction avec 14-3-3 avant activation |
| Thr48/Thr67/ Ser205 |
CDK1, Plk1 | Transition G2/M |
Phosphorylations cumulatives stabilisant la forme active de Cdc25C et favorisant sa translocation nucléaire |
| Ser285/Ser285-Ser287 (zone terminale) |
MAP kinases/ Chk1 |
Réponse au stress cellulaire |
Modulation de l'activité phosphatase selon l'état du cycle et des signaux extracellulaires |
Réponse aux dommages de l’ADN
Si l’ADN est endommagé ou si la réplication est incomplète, le checkpoint G2/M bloque l’activation du MPF afin d’éviter toute entrée prématurée en mitose.
1. La détection des lésions repose principalement sur deux capteurs majeurs (Human single-stranded DNA binding proteins are essential for maintaining genomic stability 2013).
-
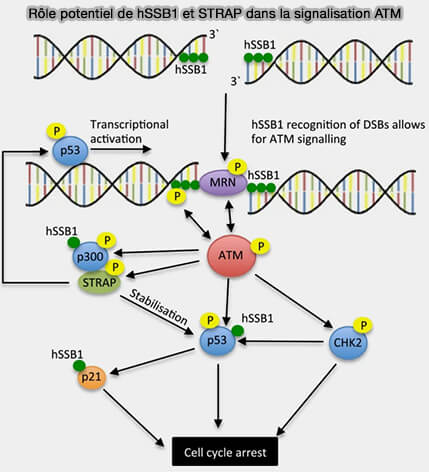
Rôle potentiel de hSSB1 et STRAP dans la signalisation ATM
(Figure : vetopsy.fr d'après Ashton et coll)
a. ATM (Ataxia-telangiectasia mutated) est activée principalement en réponse aux cassures double brin (DSB).
Cette voie conduit à l’activation préférentielle de Chk2, avec des recouvrements contextuels possibles avec Chk1 selon la nature et l’intensité du stress génomique.
b. ATR (Ataxia Telangiectasia and Rad3 related) est activée par l’accumulation d’ADN simple brin recouvert de RPA, typiquement générée lors du stress réplicatif et du blocage des fourches de réplication (
Cette voie conduit à l’activation préférentielle de CHK1.
Remarque : la réponse aux dommages de l’ADN est principalement orchestrée par la voie ATM/CHK2 et la voie ATR/CHK1, ces deux axes coopérant avec DNA-PKcs, p53 et les voies de réparation spécialisées pour maintenir la stabilité génomique.
c. Les kinases Chk1 et Chk2 phosphorylent ensuite Cdc25C sur les sites inhibiteurs, notamment Ser216 ce qui entraîne :
- son interaction avec les protéines 14-3-3,
- sa rétention cytoplasmique,
- son incapacité à déphosphoryler CDK1, bloquant ainsi l’entrée en mitose.
2. En outre, l’inhibition de Cdc25 entraîne d’autres effets.
a. Elle renforce l’action de Wee1 et Myt1 (PKMYT1), qui maintiennent CDK1 phosphorylée sur Thr14 et Tyr15, assurant ainsi une inactivation stricte de CDK1 tant que les anomalies persistent.
b. La signalisation ATR/Chk1 et ATM/Chk2 inhibe également Cdc20 et Cdh1, les coactivateurs du complexe APC/C, ce qui :
- empêche toute activation prématurée de l’APC/C (
Cdc20 et Cdh1 lors de dommages à l'ADN).
- évite la dégradation anticipée des cyclines B, d’Aurora A, de Plk1 et de la géminine.
c. Elle ralentit ou arrête le cycle, laissant à la cellule le temps nécessaire pour :
- réparer les cassures,
- stabiliser les fourches,
- éliminer les anomalies avant l’entrée en mitose.
3. En cas de dommages persistants, la cellule engage une réponse en deux volets distincts.
a. Le cycle s'arrête.
- ATR/Chk1 provoque un arrêt en S/G2 principalement via l’inhibition de Cdc25.
- ATM/Chk2 peut bloquer la progression en G1, S ou G2 en inhibant les CDK correspondantes, soit par l’axe p53/p21CIP1, soit par l’inhibition de Cdc25, selon la phase du cycle concernée.
b. L’apoptose, lors de lésions irréparables, dépend principalement de la voie ATM-Chk2, qui implique une activation de p53 distincte de celle utilisée pour l’arrêt du cycle.
- Pour l’arrêt du cycle, p53 induit l’expression de p21CIP1, ce qui bloque la progression en G1, S ou G2.
- Pour l’apoptose, p53 déclenche l’expression de BAX, PUMA, NOXA, qui activent la voie mitochondriale de l’apoptose ou voie intrinsèque et conduisent à la mort cellulaire.
Point de contrôle du fuseau (SAC), assuré par le complexe MCC
Le point de contrôle du fuseau repose sur le SAC (Spindle Assembly Checkpoint), un système de surveillance qui empêche l’activation de l’APC/C tant que l’attachement des microtubules aux kinétochores n’est pas correctement établi.
Lorsque des kinétochores demeurent libres ou soumis à une tension insuffisante, le complexe MCC (Mitotic Checkpoint Complex) se forme, neutralise Cdc20 et empêche la transition métaphase-anaphase, garantissant une ségrégation chromosomique fidèle et prévenant l’instabilité génomique.
Ouverture vers la régulation globale du cycle
Les checkpoints décrits ici correspondent aux mécanismes de surveillance immédiate qui contrôlent directement l’intégrité du génome, la progression de la réplication et la ségrégation chromosomique.
Ils ne constituent toutefois qu’un niveau du contrôle global du cycle cellulaire, qui intègre également des mécanismes plus larges liés à la compétence proliférative, à l’état physiologique de la cellule et à son environnement.

Ces dispositifs relèvent d’une régulation plus globale du cycle cellulaire et sont présentés dans la page consacrée à la régulation du cycle cellulaire.
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


