Cycle cellulaire
Interphase : préparation à la division cellulaire
Phase S : réplication de l'ADN
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La phase S du cycle cellulaire correspond à la période où la cellule réplique intégralement son ADN, assurant la duplication fidèle du génome avant la division cellulaire.
Le cycle cellulaire comprend plusieurs phases qui sont sous la dépendance des complexes cyclines/CDK.
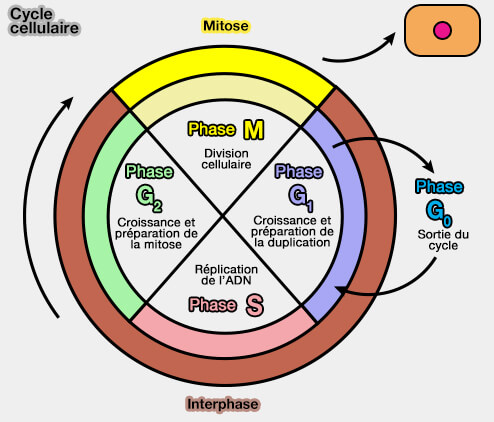
(Figure : vetopsy.fr d'après Zephris)
L’interphase, phase préparatoire du cycle cellulaire au cours de laquelle la cellule croît, réplique son ADN et prépare tous les éléments nécessaires à la division, est divisée en trois phases.
- La phase G1 (de l'anglais growth, croissance ou gap, intervalle ou espace), est la première phase de croissance cellulaire (2n, 2c).
- La phase S (de l'anglais synthesis, synthèse) correspond à la réplication complète du matériel génétique (2n, 4c).
- La phase G2 est la dernière étape de l’interphase, qui a pour fonction principale de préparer la cellule à la mitose en vérifiant la complétude et l’intégrité du génome, tout en assurant la mise en place des structures nécessaires à la division cellulaire (2n, 4c).
Phase S
Réplication de l'ADN
La phase S (de l'anglais synthesis, synthèse) correspond à la réplication complète du matériel génétique.
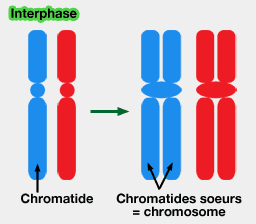
(Figure : vetopsy.fr)
1. Chaque chromosome passe de 1 chromatide à 2 chromatides dites soeurs (2n, 4c).
La phase S est essentielle pour la fidélité génétique, car toute erreur de réplication peut entraîner des mutations ou des anomalies chromosomiques.
2. La chromatine reste majoritairement sous forme d’euchromatine, configuration peu condensée, qui permet un accès efficace aux enzymes de réplication et aux facteurs de réparation.
Certaines régions d’hétérochromatine plus compactes sont répliquées plus tardivement, reflétant l’organisation structurale du génome.
Régulations par les cyclines/CDK
La progression de la phase S est contrôlée de manière séquentielle par les complexes cycline E/CDK2, puis cycline A/CDK2 et cycline A/CDK1, dont l’activation résulte des événements initiés en fin de G1.
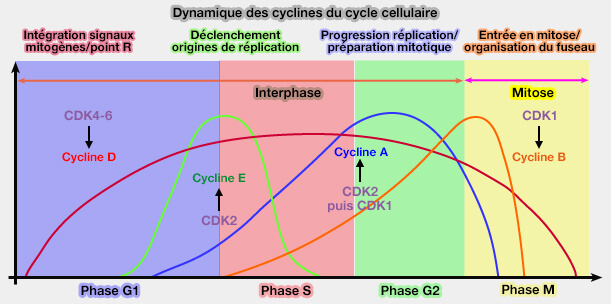
(Figure : vetopsy.fr)
1. En phase G1, les origines de réplication ont été rendues compétentes par l’assemblage des licensing factors pour former le complexe de pré‑réplicatif (pré-RC).
- Cet assemblage définit un état d’origine " licenciée ", littéralement mise en capacité, mais encore incapable d’initier la réplication.
- En fin de G1, la libération du facteur de transcription E2F consécutive à la phosphorylation de Rb par les complexes cycline D/CDK4-6 induit la transcription de la cycline E (
rôles des cyclines/CDK de G1).
L’assemblage des complexes cycline E/CDK2 constitue l’événement terminal du passage du point de restriction (R) et prépare immédiatement l’amorçage des origines de réplication.
2. Au début de la phase S, l’activité des complexes cycline E/CDK2 puis cycline A/CDK2 permet l’activation fonctionnelle des origines par la phosphorylation de facteurs clés, en particulier Treslin (Mechanisms and regulation of DNA replication initiation in eukaryotes 2017).
a. La phosphorylation de Treslin constitue un signal d’activation central des origines licenciées.
- Sans phosphorylation de Treslin, le complexe MCM2-7 est chargé sur l’ADN, mais l’origine demeure inactive.
- Treslin phosphorylé permet le recrutement de TopBP1 (DNA topoisomerase 2-binding protein 1), adaptateur essentiel qui coordonne le recrutement des composants nécessaires à l’activation de l’hélicase.
Remarque : à ce stade, les composants du pré-RC initial, notamment le complexe ORC ainsi que Cdc6 et Cdt1, ont été fonctionnellement inactivés et dissociés des origines par phosphorylation dépendante des complexes cycline E/CDK2 puis cycline A/CDK2, laissant comme support principal le complexe MCM2-7 chargé sur l’ADN.
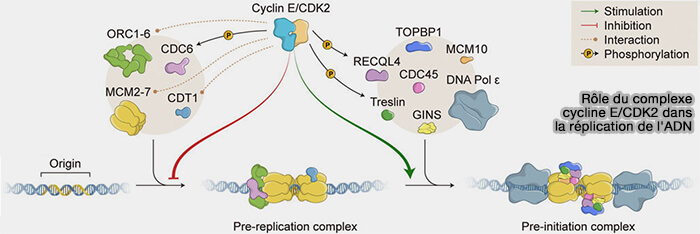
(Figure : vetopsy.fr d'après Fagundes et Teixeira)
b. Ce complexe Treslin-TopBP1 favorise ensuite le recrutement de Cdc45 sur le complexe MCM2-7 chargé sur l’ADN, résidu fonctionnel du complexe pré-réplicatif (pré-RC) .
c. Parallèlement, le complexe GINS est recruté et s’associe au MCM et à Cdc45 (The structural basis for MCM2–7 helicase activation by GINS and Cdc45 2014).

L’assemblage coordonné de Cdc45, du complexe MCM2-7 et de GINS conduit à la formation du complexe CMG (Cdc45-MCM-GINS), qui correspond à l’hélicase réplicative active et marque l’engagement irréversible de l’origine dans la réplication.
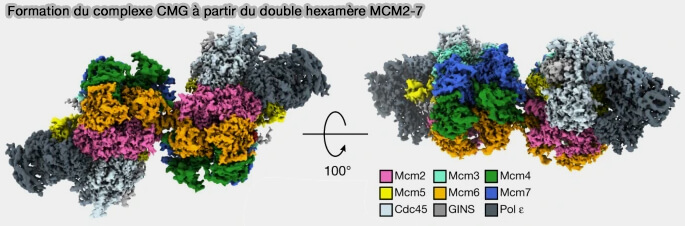
(Figure : vetopsy.fr d'après Lewis et coll)
3. L’activation du complexe CMG entraîne l’ouverture locale de la double hélice d’ADN au niveau des origines activées et la formation de deux fourches de réplication divergentes, structures en Y au sein desquelles s’organise la synthèse coordonnée des nouveaux brins.
a. Le complexe CMG (Cdc45-MCM-GINS) constitue le moteur central de la fourche de réplication. (Reconstitution of a eukaryotic replisome reveals suppression mechanisms that define leading/lagging strand operation 2015).
Il progresse le long de l’ADN simple brin matrice et assure le déroulement continu de la double hélice, imposant la polarité et la dynamique de chaque fourche.
b. La primase associée à l’ADN polymérase α, à proximité immédiate de l’hélicase, initie la synthèse en déposant de courtes amorces d’ARN, fournissant les extrémités 3′-OH nécessaires au démarrage de la réplication.
c. Les ADN polymérases assurent ensuite l’élongation des brins néo-synthétisés.
- Sur le brin directeur, l’ADN polymérase ε assure une synthèse continue, strictement couplée à la progression de l’hélicase CMG.
- Sur le brin retardé, l’ADN polymérase δ prend le relais de la primase et synthétise l’ADN de manière discontinue sous forme de fragments d'ADN appelés fragments d’Okazaki.
Le brin retardé résulte de la contrainte directionnelle des ADN polymérases, qui ne synthétisent l’ADN que dans le sens 5′ → 3′. En raison de l’antiparallélisme des deux brins parentaux, ce brin ne peut être répliqué que de manière discontinue à mesure que la fourche de réplication progresse.
d. L’ADN ligase relie ces fragments sur le brin retardé, permettant la formation d’un brin continu et la progression efficace et coordonnée des fourches de réplication le long du génome.
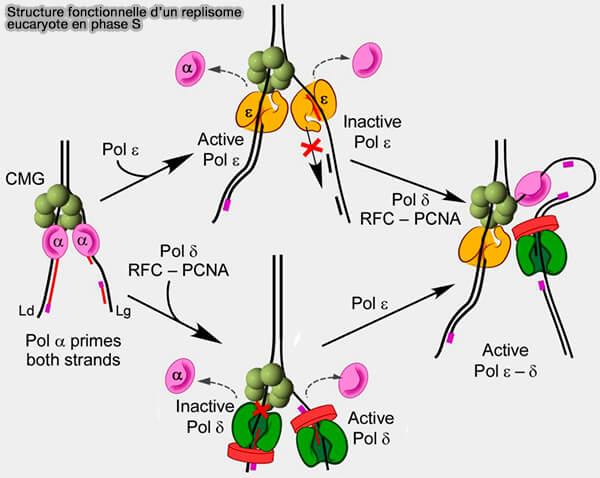
(Figure : vetopsy.fr d'après Georgescu et coll)
4. Ce mécanisme permet une activation contrôlée et progressive des origines, garantissant que l’ensemble du génome ne soit répliqué une seule fois et de manière coordonnée au cours de la phase S, c’est-à-dire sans re-licensing. des origines déjà engagées.

Le checkpoint S, étudié dans un chapitre spécifique, assure le maintien de l’unicité de la réplication en bloquant toute réactivation aberrante des origines en cas de stress de réplication ou de dommages à l’ADN, et en empêchant la progression vers la phase G2 tant que ces anomalies persistent.
3. La cycline A est ensuite induite sous le contrôle d’E2F et remplace progressivement la cycline E au sein des complexes CDK2.
a. L’induction de la cycline A s’accompagne de l’extinction progressive de l’activité transcriptionnelle d’E2F, ce qui met fin au programme G1/S et stabilise l’engagement en phase S.
b. L’assemblage des complexes cycline A/CDK2 prend alors le relais de cycline E/CDK2 pour :
- maintenir l’activité des fourches de réplication,
- coordonner la progression des fourches à travers l’ensemble du génome,
- influencer l’activité des ADN polymérases et des complexes associés afin d’assurer une vitesse de réplication constante et équilibrée en fonction des besoins locaux,
- prévenir toute réactivation des origines déjà engagées, en imposant un état réfractaire au rechargement du pré-RC.
5. En fin de phase S, l’activité du complexe cycline A/CDK2 diminue progressivement, permettant l’accumulation des complexes cycline A/CDK1 et cycline B/CDK1 (MPF) caractéristiques de la phase G2, qui prépareront l’entrée en mitose.
| Étape | Acteurs principaux | Événements clés | Conséquence fonctionnelle |
|---|---|---|---|
| Transition G1 ➞ S |
|
|
Passage du point R et amorçage des origines de réplication |
| Début de la phase S |
|
|
|
| Fourches de réplication actives |
|
|
Progression efficace et fidèle des fourches |
| S intermédiaire (prise de relais) | Cycline A/CDK2 | Remplacement progressif de cycline E/CDK2 par cycline A/CDK2 |
Coordination de la vitesse et de la progression des fourches à travers le génome |
| Contrôle de la réplication |
|
|
|
| Réponse aux dommages ou au stress |
|
|
|
| Fin de la phase S |
|
|
Préparation de la transition S ➞ G2 en vue des contrôles pré-mitotiques |
Phase G2 : préparation à la mitose
La phase G2 est la dernière étape de l’interphase, qui a pour fonction principale de préparer la cellule à la mitose en vérifiant la complétude et l’intégrité du génome, tout en assurant la mise en place des structures nécessaires à la division cellulaire (2n, 4c).
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


