Cycle cellulaire
Cyclines : cycline B et complexe cycline B/CDK1 (MPF)
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La cycline B active CDK1 pour former le MPF, moteur enzymatique de l’entrée en mitose, contrôlant la prophase, la métaphase et la transition métaphase-anaphase.
L’activation progressive du complexe cycline B/CDK1 en fin de G2, son accumulation nucléaire, puis la dégradation ciblée de la cycline B à la transition métaphase-anaphase gouvernent l’ensemble des transitions mitotiques.
La cycline B constitue ainsi un véritable commutateur moléculaire orchestrant l’organisation du noyau, du fuseau et des chromosomes.
Cette fonction repose non seulement sur la dynamique d’expression de la cycline B, mais aussi sur une régulation spatiale fine du complexe cycline B/CDK1, avec une activation initialement cytoplasmique, puis une translocation nucléaire coordonnée au franchissement du point de contrôle G2/M.
Structure et isoformes de la cycline B
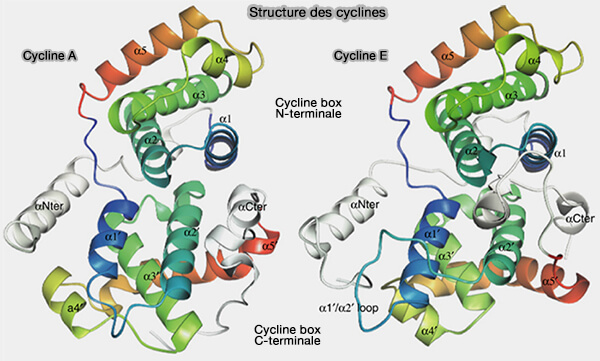
La cycline B appartient à la famille des cyclines mitotiques et partage avec elles une architecture structurale conservée caractérisée par un repliement de type cyclin fold constitué de deux boîtes à cycline caractéristiques de sa famille, dont l’organisation tridimensionnelle est nécessaire à l’interaction avec les CDK et à leur activation.
1. Chez les mammifères, plusieurs isoformes coexistent, principalement les cyclines B1 et B2.
- La cycline B1 est majoritaire et s’accumule principalement dans le cytoplasme, puis dans le noyau à l’entrée en mitose, où elle joue un rôle central dans le déclenchement des événements mitotiques.
- La cycline B2 présente une localisation plus associée aux membranes internes (notamment appareil de Golgi et réticulum endoplasmique), et contribue davantage à des régulations locales, bien que leurs fonctions convergent toutes deux vers l’activation de CDK1.
(Figure : vetopsy.fr d'après Honda et coll)
1. La région N-terminale porte :
- un motif de destruction de type D-Box, indispensable à sa reconnaissance par l’APC/CCdc20 en métaphase et responsable de sa dégradation rapide lors de la transition métaphase-anaphase,
- un signal d’export nucléaire (NES) régulé par phosphorylation,
- un signal de localisation nucléaire (NLS) activé en fin de G2, permettant l’accumulation nucléaire indispensable au déclenchement de la prométaphase.
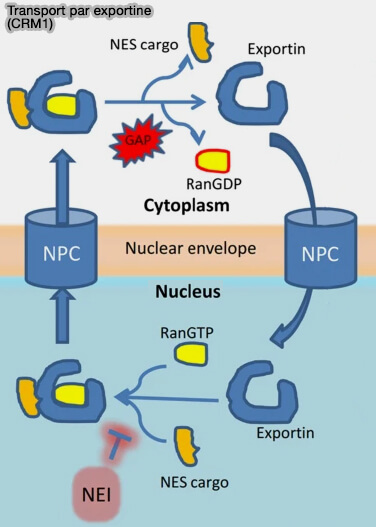
(Figure : vetopsy.fr d'après Sun et coll)
a. CRM1 (Exportine-1, XPO1) est une exportine nucléaire dont la fonction, en présence de Ran-GTP, est de reconnaître les protéines porteuses d’un signal NES et de les exporter du noyau vers le cytoplasme à travers le pore nucléaire (Inhibiting cancer cell hallmark features through nuclear export inhibition 2016).
CRM1 maintient le complexe cycline B/CDK1 majoritairement cytoplasmique en interphase.
b. En fin de G2, la phosphorylation de la cycline B et de CDK1 par CDK1 elle-même et par Plk1 altère la reconnaissance du NES par CRM1, inhibe l’export nucléaire et favorise l’accumulation nucléaire rapide du complexe.

Ce basculement de localisation constitue un mécanisme clé de verrouillage moléculaire de l’entrée en mitose.
2. Le domaine C-terminal de la cycline B constitue la seconde boîte à cycline du repliement conservé des cyclines (cyclin fold), principalement composé d’hélices α organisées de manière comparable au domaine N-terminal, et contribue à la stabilité globale de la protéine et du complexe cycline B/CDK1.
Remarque : le complexe cycline A/CDK2 existe, mais :
- elle agit plus précocement, en fin G2/début prophase,
- elle devient fonctionnellement secondaire une fois que le complexe cycline B/CDK1 est pleinement actif, et la cycline A est détruite dès la prométaphase par l’APC/CCdc20.
Complexe cycline B/CDK1 (MPF)
Le complexe cycline B/CDK1, également désigné MPF, constitue le moteur enzymatique central de l’entrée en mitose.
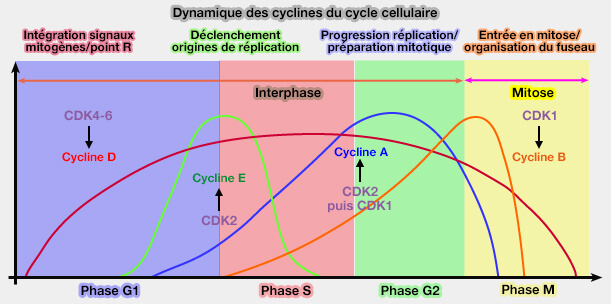
(Figure : vetopsy.fr)
Activation du complexe cycline B/CDK1 (MPF)
L’entrée en prophase repose sur l’activation progressive du MPF (Maturation Promoting Factor), complexe hétérodimérique formé par (MPF-based meiotic cell cycle control: Half a century of lessons from starfish oocytes 2018) :
- CDK1 (Cyclin-Dependent Kinase 1), aussi appelée Cdc2,
- la cycline B qui lui confère sa spécificité de phase et sa régulation temporelle.
Le MPF a été découvert lors de l’étude du déblocage de la méiose II ovocytaire après la fécondation chez le Xénope, d’où son appellation de facteur de maturation.
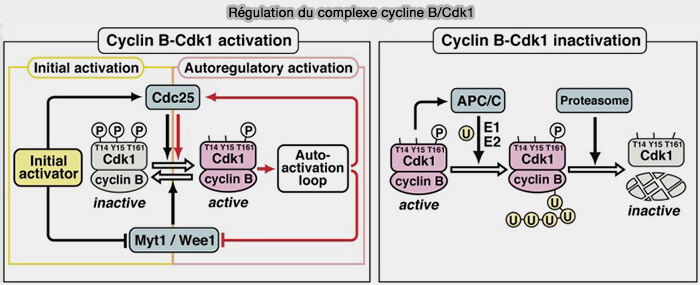
(Figure : vetopsy.fr d'après Kishimoto)
1. Une fois la cellule engagée en phase S, après le point R, l’expression et l’accumulation de la cycline B relèvent d’un contrôle endogène du cycle et non plus d’un contrôle par les signaux mitogènes.
a. La régulation transcriptionnelle devient alors cyclique et dépend de facteurs activés au cours des phases S et G2, notamment FOXM1, B-Myb et certains E2F tardifs selon le contexte cellulaire.
b. La cycline B s’accumule également en raison d’une stabilisation progressive de la protéine.
- Sa dégradation reste faible pendant les phases S et G2, ce qui permet une accumulation nette par simple déséquilibre entre la synthèse et la dégradation.
- Cette accumulation est rendue possible par l’inactivation de l’APC/CCdh1 après la phase G1, ce qui autorise la stabilité des cyclines mitotiques, en particulier la cycline A, puis la cycline B.
c. En revanche, l’activation fonctionnelle du complexe cycline B/CDK1 demeure strictement contrôlée par des mécanismes post-traductionnels,
- incluant l’inhibition de CDK1 par Wee1 et Myt1 (PKMYT1),
- l’activation par Cdc25C,
- la régulation de la localisation nucléocytoplasmique via les signaux NES/NLS,
- des boucles de rétroactivation postives et négatives.
2. En début de prophase, l’activité du MPF est déjà croissante, car son activation a été amorcée en phase G2 par la phosphatase Cdc25C, qui déphosphoryle CDK1 au sein du complexe cycline B/CDK1 préexistant et permet son activation enzymatique (
Cette montée d’activité déclenche les premières phosphorylations mitotiques qui initient les transformations caractéristiques de la prophase, i.e. condensation chromosomique, désorganisation progressive de la lamina, maturation des centrosomes et réorientation globale de la cellule vers l’état mitotique (
3. Peu avant la prométaphase, le complexe cycline B/CDK1 phosphorylé devient nucléaire.
a. L’activation initiale du MPF dans le cytoplasme entraîne la phosphorylation de la cycline B sur plusieurs sérines, i.e. Ser133, Ser147, Ser155 chez les mammifères.
- Ces phosphorylations inhibent le signal d’export (NES) et renforcent l’efficacité du NLS.
- Le complexe s’accumule alors massivement dans le noyau, entraînant une montée rapide de l’activité kinase au sein de ce compartiment.
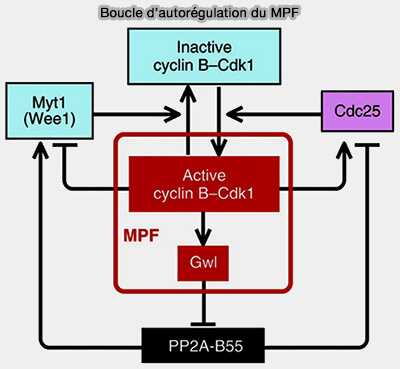
(Figure : vetopsy.fr d'après Hara et coll)
b. Cette importation nucléaire est essentielle pour déclencher les événements mitotiques précoces.
c. Ainsi, la translocation nucléaire du MPF précède de peu la rupture de l’enveloppe nucléaire, et en constitue un élément déclencheur majeur.
4. L’entrée du MPF dans le noyau est amplifiée par les kinases relais cytoplasmiques.
a. Plk1 et Aurora A qui augmentent la vitesse de diffusion du signal mitotique depuis le centre vers la périphérie.
- MPF active Plk1, qui à son tour active Cdc25 et inhibe Wee1, renforçant la boucle de rétroactivation positive.
- Plk1 et Aurora A sont concentrées aux centrosomes et le long des microtubules, ce qui favorise la propagation spatiale du signal mitotique et accélère l’activation coordonnée de l’ensemble du cytoplasme.
b. Ces boucles accélèrent la transition vers la prométaphase en contribuant à la coordination spatio-temporelle de l’entrée en mitose (
5. Lorsque la phosphorylation cumulée atteint un seuil critique, la rupture de l’enveloppe nucléaire provoque ensuite l’homogénéisation des compartiments nucléaire et cytoplasmique, et la diffusion uniforme de l’activité MPF.

En quelques minutes, l’activité kinase devient maximale dans l’ensemble du cytoplasme et du noyau, marquant l’entrée en prométaphase et la mise en place d’un état mitotique pleinement établi.
6. Après le déclenchement de la mitose, le MPF reste actif durant la prophase et la métaphase pour maintenir la métaphase, la structure du fuseau et l’activation des kinases relais.
Sa dégradation surviendra surtout à la transition métaphase/anaphase, déclenchée par l’APC/CCdc20.
Actions chronologiques du MPF
L’activité du MPF s’exprime selon une séquence ordonnée qui suit fidèlement les transformations structurales de la prophase à la métaphase.
Chaque étape correspond à la phosphorylation coordonnée de substrats spécifiques, immédiatement suivie de leurs effets fonctionnels.
MPF et prophase
1. En prophase, l’entrée dans l’état mitotique repose sur une augmentation progressive de l’activité du complexe cycline B/CDK1 (MPF), déjà engagé en fin de G2.
Cette montée d’activité ne déclenche pas un événement unique, mais une cascade coordonnée de phosphorylations qui imposent simultanément des changements nucléaires, chromosomiques et cytoplasmiques.
a. L’activité initiale du MPF cible un large spectre de substrats structuraux et régulateurs, ce qui permet :
- l'amorce de la condensation de la chromatine en chromosomes, par la phosphorylation des histones, notamment H1 et H3 (Ser 10) et des condensines (kleisines CAP-D2, CAP-H),
- la levée progressive de la cohésion sur les bras chromosomiques, par phosphorylation de composants de la cohésine II, notamment la sous-unité HEAT SA2 et WAPL, favorisant leur dissociation dépendante de WAPL,
- le début de la désorganisation de la lamina, sans rupture complète de l'enveloppe nucléaire, par phosphorylation des lamines A/C et B,
- la maturation progressive des centrosomes pour la formation du fuseau mitotique, par phosphorylation de protéines du matériel péricentriolaire (PCM), telles que PCNT (péricentrine), CEP192, NEDD1 (GCP-WD),
- la réorganisation du cytosquelette d’actine, par phosphorylation de protéines d’ancrage et de remodelage de l’actine, comme les protéines ERM (ezrine, radixine et moésine) et la cofiline,
- la réduction des activités transcriptionnelles nucléaires, par phosphorylation de facteurs de transcription et de la machinerie transcriptionnelle, notamment TFIIH, TFIID, ARN polymérase II (CTD),
- le maintien du checkpoint G2/M, via la persistance d’un signal MPF, qui s’accompagne notamment de la répression fonctionnelle de p53, de l’inactivation des voies ATR/Chk1 et ATM/Chk2 et du maintien de Cdc25 dans un état actif sous l’effet des boucles de rétroactivation CDK1/Plk1.
b. Ces phosphorylations établissent un état mitotique global stable, tout en maintenant l’inactivation des systèmes de surveillance tant que l’intégrité du génome n’est pas compromise.
2. En fin de prophase, ce n’est plus la quantité d’activité MPF qui change, mais sa localisation : le complexe cycline B/CDK1 se concentre préférentiellement dans le noyau, ce qui focalise son activité sur les substrats nucléaires.
- La phosphorylation de la cycline B inhibe son signal d’export nucléaire (NES), ce qui bloque son export dépendant de CRM1 et entraîne une accumulation rapide du complexe cycline B/CDK1 dans le noyau par simple rétention nucléaire.
- Elle est encore amplifiée par des boucles impliquant Plk1 et Aurora A.
Prométaphase : rupture de l’enveloppe nucléaire
et synchronisation globale
1. En prométaphase, lorsque le MPF atteint une activité maximale dans le noyau, la phosphorylation accumulée des lamines et des complexes du pore nucléaire (NPC) déclenche la rupture de l’enveloppe nucléaire.
Cette rupture homogénéise instantanément le contenu nucléaire et cytoplasmique, permettant la diffusion uniforme du MPF et assurant la synchronisation des événements mitotiques.
2. Le MPF maintient :
- la condensation chromosomique,
- la dynamique des centrosomes et du fuseau,
- la capture initiale des kinétochores par les microtubules par la corona fibreuse.
Métaphase : maintien de la compaction et stabilité du fuseau
En métaphase, l’activité du complexe cycline B/CDK1 (MPF) demeure élevée et homogène dans la cellule.
1. Ce niveau d’activité ne sert plus à initier des transformations majeures, mais à verrouiller l’état mitotique tant que les conditions mécaniques ne sont pas validées.
a. Le MPF prolonge et renforce les processus engagés en prométaphase.
- Il maintient la condensation maximale chromosomique en phosphorylant de manière continue l’histone H3 (et secondairement de H1) et les condensines, empêchant toute décondensation prématurée avant la séparation des chromatides soeurs.
- Il stabilise l’architecture du fuseau mitotique par la phosphorylation de protéines associées aux microtubules et aux pôles, notamment des composants du matériel péricentriolaire, i.e. PCNT (péricentrine), CEP192, CDK5RAP2 (CEP215), et des MAP régulant la dynamique microtubulaire, i.e. XMAP215.
/ch-TOG et TACC3, ce qui soutient la nucléation, l’alignement et la cohésion fonctionnelle des pôles, garantissant la géométrie bipolaire nécessaire à la métaphase.
b. Le MPF empêche l’entrée en anaphase tant que le point de contrôle du fuseau (SAC) n’est pas levé, en maintenant un contexte enzymatique incompatible avec l’activation effective de l’APC/CCdc20.
2. Ainsi, en métaphase, le complexe cycline B/CDK1 agit comme un verrou enzymatique, assurant la stabilité structurale et temporelle de l’état mitotique jusqu’à ce que la biorientation complète des chromosomes autorise la transition métaphase-anaphase.
Transition métaphase–anaphase et extinction progressive du MPF
1. L’activation de l’APC/CCdc20 à la transition métaphase-anaphase constitue un point de bascule majeur.
- Elle déclenche la séparation des chromatides sœurs par la dégradation de la sécurine et l’activation de la séparase.
- Elle initie simultanément l’extinction progressive du MPF par la dégradation de la cycline B.
L’APC/C activé par Cdc20 reconnaît la cycline B via sa D-Box et la polyubiquitine, conduisant à sa destruction rapide par le protéasome.
2. La chute durable de l’activité cycline B/CDK1 conditionne l’ensemble des événements de sortie de mitose, en particulier la télophase, en autorisant la déphosphorylation coordonnée des substrats mitotiques.
Cette extinction progressive du MPF permet :
- la reformation de l'enveloppe nucléaire,
- la décondensation chromosomique,
- le désassemblage contrôlé du fuseau mitotique.
Le tableau suivant synthétise la dynamique chronologique de l’activité du complexe cycline B/CDK1 (MPF) depuis la fin de G2 jusqu’à la transition métaphase-anaphase, en reliant les événements cellulaires aux fonctions enzymatiques correspondantes.
| Phase | Événements clés | Rôle du MPF/ kinases |
Notes |
|---|---|---|---|
| G2 |
|
|
|
| Fin de G2/ début prophase |
|
|
|
| Prophase |
|
|
|
| Fin prophase/ prométaphase |
|
|
|
| Métaphase |
|
|
|
| Transition métaphase- anaphase |
|
|
|
Retour aux cyclines
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


