Cycle cellulaire
Cyclines : cycline E
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La cycline E déclenche irréversiblement l’entrée en phase S en activant CDK2 et en contrôlant l’initiation des origines de réplication.
Structure et isoformes de la cycline E
La cycline E appartient à la famille des cyclines mitotiques et partage avec elles une architecture structurale conservée caractérisée par un repliement de type cyclin fold constitué de deux boîtes à cycline caractéristiques de sa famille, dont l’organisation tridimensionnelle est nécessaire à l’interaction avec les CDK et à leur activation.
1. Chez les mammifères, on trouve deux isoformes, la cycline E1 (CCNE1) et la cycline E2 (CCNE2).
- Ces deux isoformes présentent des fonctions largement redondantes dans le contrôle de la transition G1/S, mais diffèrent par leur niveau d’expression selon les tissus et par leur régulation post-traductionnelle.
- La cycline E1 est généralement considérée comme la forme dominante dans la majorité des cellules prolifératives.
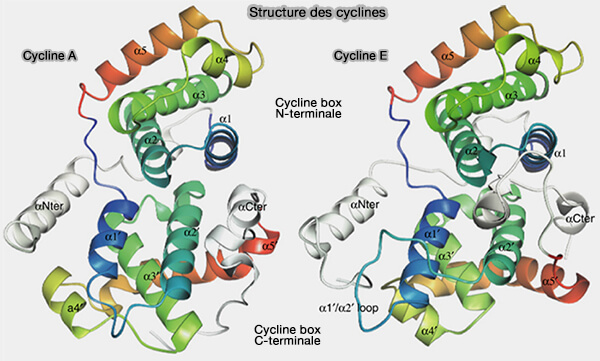
(Figure : vetopsy.fr d'après Honda et coll)
La cycline E se distingue des autres cyclines du cycle par plusieurs caractéristiques structurales propres à ses régions périphériques.
1. La région N-terminale de la cycline E est riche en motifs de dégradation dépendants de phosphorylation, appelés phospho-dégrons, qui conditionnent sa reconnaissance par le complexe SCFFbxw7.
a. Ces motifs incluent :
- un motif CPD (Cdc4 phosphodegron),
- plusieurs sites de phosphorylation dépendants de CDK2 et de GSK3, qui, une fois phosphorylés, permettent l’interaction avec la protéine Fbxw7 et déclenchent la dégradation protéasomale de la cycline E.
b. Cette organisation confère à la cycline E une demi-vie courte et un contrôle particulièrement strict de son accumulation au cours de la fin de la phase G1.
2. Le domaine C-terminal et les surfaces périphériques de la cyclin fold de la cycline E présentent une organisation adaptée à l’interaction préférentielle avec CDK2, expliquant que la cycline E ne forme pas de complexe fonctionnel stable avec CDK1 dans des conditions physiologiques.
La cycline E possède un site de docking de type Cy permettant la reconnaissance des substrats porteurs d’un motif RXL, avec une spécificité de substrat distincte de celle des cyclines A et B.
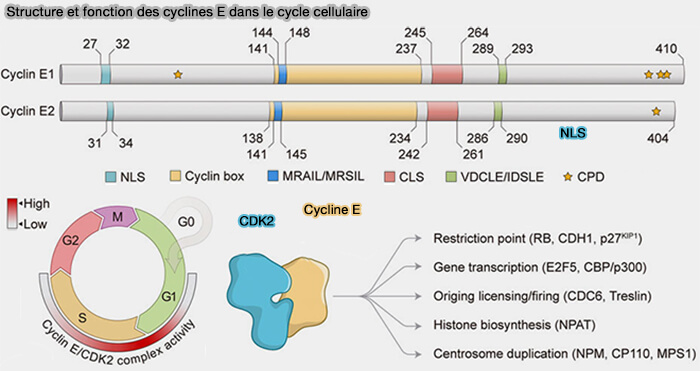
(Figure : vetopsy.fr d'après Fagundes et Teixeira)
3. Une particularité de la cycline E est l’existence, dans de nombreux contextes tumoraux, de formes tronquées de bas poids moléculaire (LMW-E, Low Molecular Weight Cyclin E).
- Ces formes résultent d’un clivage protéolytique anormal des régions périphériques et conservent le cœur cyclin fold fonctionnel, ce qui produit une cycline E plus stable, partiellement résistante à la dégradation par SCF, associée à une hyperactivité de CDK2.
- Ces formes tronquées constituent une signature structurale et fonctionnelle propre aux situations pathologiques et sont fortement associées à l’instabilité génomique et à l’agressivité tumorale.
Complexe cycline E/CDK2
Activation du complexe cycline E/CDK2
L’activation du complexe cycline E/CDK2 constitue l’événement enzymatique décisif du passage du point de restriction (R) de la phase G1 et de l’engagement irréversible de la cellule dans la phase S.
1. L’induction de l’expression de la cycline E dépend de l’activation des facteurs de transcription E2F, elle-même contrôlée par la cascade signaux mitogènes ➞ cycline D/CDK4-6 ➞ phosphorylation de Rb ➞ libération d’E2F (

Cette induction marque la perte de dépendance aux signaux mitogènes externes et l’entrée dans un programme autonome de progression du cycle.
2. La cycline E nouvellement synthétisée s’associe à CDK2, formant un complexe initialement peu actif, dont la maturation dépend de plusieurs mécanismes régulateurs.
a. L’association à la cycline induit le réarrangement structural de CDK2, i.e. réorganisation de l’hélice αC et de la boucle T, rendant le site catalytique fonctionnel.
La phosphorylation de la boucle T de CDK2 (Thr160) par la CAK (cycline H/CDK7/Mat1) stabilise la conformation active et confère au complexe son efficacité catalytique maximale.
b. Toutefois, l’activité du complexe cycline E/CDK2 demeure freinée par plusieurs mécanismes régulateurs :
- la phosphorylation inhibitrice de CDK2 par Wee1/Myt1 (PKMYT1),
- l’action des CKI (CDK inhibitors) de la famille CIP/KIP (p21, p27).
3. La levée de cette inhibition repose notamment sur :
- la phosphorylation de p27 par le complexe cycline E/CDK2 (Thr187) lui-même, qui favorise sa dissociation du complexe puis son ubiquitination par SCFSKP2,
- la diminution de p21 en fin de G1, principalement liée à l’extinction progressive de l’activité de p53 sous l’effet des signaux mitogènes,
- la déphosphorylation activatrice de CDK2 par Cdc25A.
4. Lorsque l’activité cycline E/CDK2 dépasse un seuil critique :
- l’activation devient auto-entretenue par des boucles de rétroactivation positives,
- la phosphorylation de Rb est amplifiée,
- l’expression d’E2F devient autonome, ce qui verrouille définitivement l’entrée en phase S.
Actions chronologiques du complexe cycline E/CDK2
L’activité du complexe cycline E/CDK2 s’exerce sur une fenêtre temporelle étroite, centrée sur la fin de G1 et le tout début de la phase S, et correspond au moment où la cellule bascule d’un état de préparation vers un état d’engagement réplicatif.
Fin de G1
En fin de phase G1, l’augmentation rapide de l’activité du complexe cycline E/CDK2 amplifie la phosphorylation de Rb, ce qui renforce la libération d’E2F et verrouille définitivement l’entrée dans la phase S.
1. Cette amplification établit une boucle de rétroactivation positive :
- plus l’activité CDK2 augmente,
- plus l’expression des gènes E2F-dépendants est stimulée,
- plus l’engagement en phase S devient irréversible.
2. Cette activité kinase marque la transition fonctionnelle entre :
- une cellule encore dépendante des signaux mitogènes, avant le point de restriction (R),
- une cellule engagée de manière autonome dans la progression du cycle.
Phase S
1. Au début de la phase S, le complexe cycline E/CDK2 participe directement à l’activation des origines de réplication préalablement licenciées durant la phase G1 (
Il agit notamment par phosphorylation de facteurs clés de l’initiation réplicative, en particulier Treslin (TICRR), permettant le recrutement de Cdc45 ainsi que du complexe GINS, conduisant à la formation du complexe CMG (Cdc45-MCM-GINS), qui correspond à l’hélicase réplicative active (Cyclin E/CDK2: DNA Replication, Replication Stress and Genomic Instability 2021).
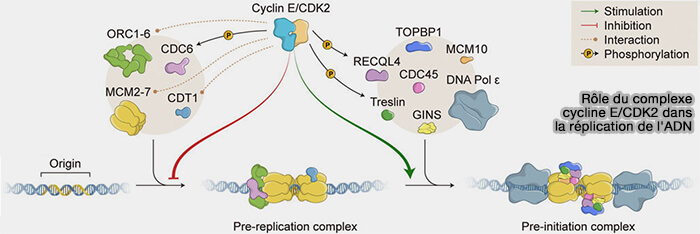
(Figure : vetopsy.fr d'après Fagundes et Teixeira)
2. Dès le début de la phase S, la cycline E est rapidement dégradée par le complexe SCFFbxw7, ce qui entraîne :
- la diminution progressive de l’activité CDK2 dépendante de la cycline E,
- la prise de relais par le complexe cycline A/CDK2, qui assurent la poursuite de la réplication en maintenant l’activité des fourches, en coordonnant leur progression et en empêchant tout re-licensing des origines déjà engagées.

Cette succession cycline E ➞ cycline A assure une continuité fonctionnelle entre le déclenchement des origines de réplication et le maintien coordonné des fourches tout au long de la phase S.
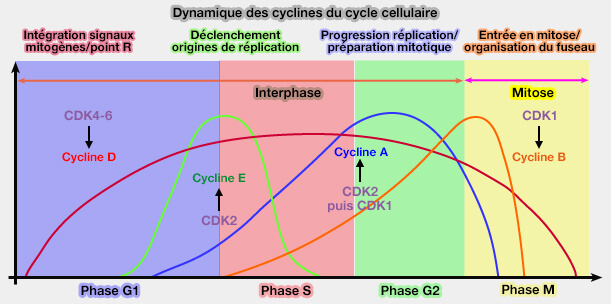
(Figure : vetopsy.fr)
Retour aux cyclines
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


