Cycle cellulaire
Cyclines : cycline A
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La cycline A coordonne la continuité du cycle cellulaire en activant successivement CDK2 puis CDK1 pour orchestrer la phase S, la phase G2 et l’entrée en mitose.
Structure et isoformes de la cycline A
La cycline A appartient à la famille des cyclines mitotiques et partage avec elles une architecture structurale conservée caractérisée par un repliement de type cyclin fold constitué de deux boîtes à cycline caractéristiques de sa famille, dont l’organisation tridimensionnelle est nécessaire à l’interaction avec les CDK et à leur activation.
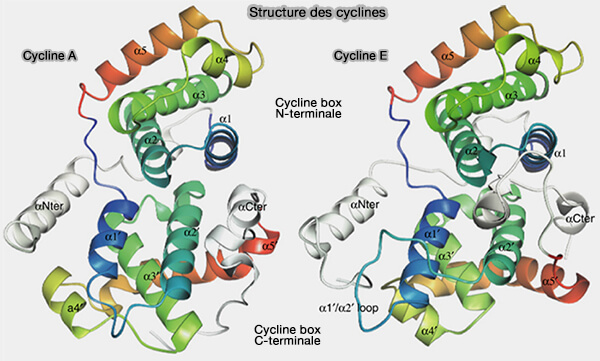
(Figure : vetopsy.fr d'après Honda et coll)
1. Chez les mammifères, deux isoformes principales sont décrites :
- la cycline A1, exprimée préférentiellement dans la lignée germinale et impliquée dans la méiose,
- la cycline A2, ubiquitaire, responsable des fonctions mitotiques dans les cellules somatiques.
2. La cycline A présente une particularité structurale notable parmi les cyclines du cycle cellulaire : son interface d’interaction avec les CDK est suffisamment permissive et conservée pour permettre l’association stable avec deux partenaires catalytiques très proches, CDK2 et CDK1.
a. Cette compatibilité repose sur :
- la conservation des résidus impliqués dans l’interface de liaison à l’hélice αC des CDK,
- une plasticité locale de certaines boucles de surface du cyclin fold, sans modification de l’architecture globale du repliement.
b. Il n’existe pas de domaines distincts dédiés à CDK2 et à CDK1 et la même surface structurale permet l’interaction avec les deux kinases.
La cycline A est majoritairement localisée dans le noyau durant la phase S et la phase G2, et sa régulation repose principalement sur ses partenaires CDK et sa dégradation précoce en mitose.
3. Les régions situées en dehors du cœur du cyclin fold de la cycline A ne portent pas de signaux de localisation nucléocytoplasmique dominants, i.e. NES ou NLS, comparables à ceux de la cycline B.
La cycline A est majoritairement nucléaire tout au long de la phase S et de la phase G2, ce qui est cohérent avec ses fonctions liées à la réplication et à la préparation précoce de la mitose.
Complexe cycline A/CDK2
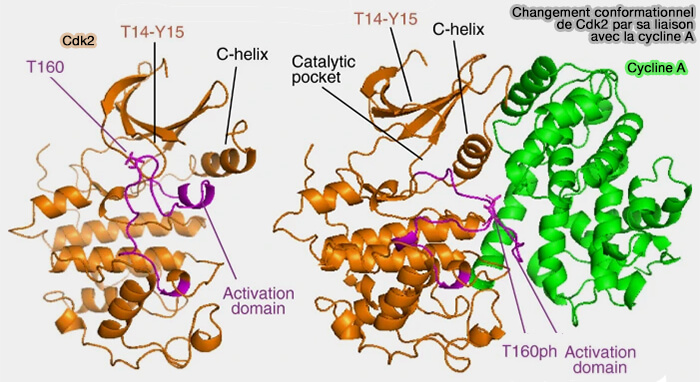
(Figure : vetopsy.fr d'après Malumbres)
Activation du complexe cycline A/CDK2
L’activation du complexe cycline A/CDK repose sur les mêmes principes généraux que ceux décrits pour les CDK, i.e. liaison à la cycline, phosphorylation de la boucle T, régulation par Cdc25A et Wee1 et Myt1 (PKMYT1), mais présente une dynamique temporelle particulière liée à la position de la cycline A dans le cycle.
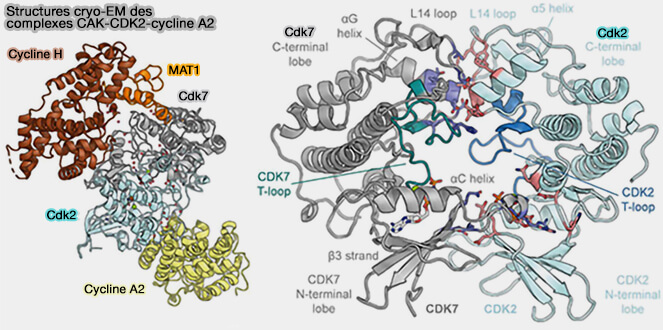
(Figure modifiée : vetopsy.fr d'après Cushing et coll)
1. L’induction de l’expression de la cycline A dépend de l’activation des facteurs de transcription E2F, elle-même contrôlée par la cascade signaux mitogènes ➞ cycline D/CDK4-6 ➞ phosphorylation de Rb ➞ libération d’E2F (

Cette induction marque la perte de dépendance aux signaux mitogènes externes et l’entrée dans un programme autonome de progression du cycle.
2. Au début de la phase S, l’accumulation progressive de la cycline A constitue le signal déclencheur permettant la formation stable des complexes cycline A/CDK2, marquant l’installation d’une activité CDK spécifique sous l’effet combiné :
- de la liaison à la cycline,
- de la phosphorylation d’activation par la CAK,
- d’un équilibre modéré entre Cdc25A et Wee1 et Myt1 (PKMYT1).
Cette activité est moins soumise à un contrôle brutal par seuil que celle du complexe cycline B/CDK1 (MPF).
3. À la transition S/G2, une fraction croissante de la cycline A s’associe à CDK1, formant un complexe cycline A/CDK1 faiblement mais détectablement actif, sans transition brutale.
Le complexe cycline A/CDK1 constitue ainsi une activité CDK1 pré-mitotique, qui prépare la cellule à l’entrée en mitose en amorçant :
- certaines phosphorylations mitotiques précoces, telles que celles des lamines A/C et B (début de désorganisation de l’enveloppe nucléaire), de la condensine II, de la topoisomérase IIα ou de l’histone H3 (Ser10),
- l’activation progressive de Plk1, notamment via sa phosphorylation sur Thr210 par Aurora A, avec une augmentation parallèle de la phosphorylation de cibles précoces comme Cdc25C et Wee1,
- la montée graduelle du réseau de rétroactivation positives, illustrée par les boucles CDK1-Cdc25 (activation) et CDK1-Wee1 (levée d’inhibition), qui conduira secondairement à l’activation explosive du complexe cycline B/CDK1.
4. L’activation de la cycline A/CDK se caractérise ainsi par :
- une montée progressive et continue de l’activité kinase,
- l’absence de seuil brutal de type commutateur,
- l’absence de mécanisme d’amplification spatiale comparable à celui observé pour la cycline B/CDK1 au niveau du noyau et des centrosomes.
5. Cette activité est intrinsèquement transitoire, car la cycline A est rapidement ciblée pour dégradation par l’APC/CCdc20 dès la prométaphase, ce qui limite strictement dans le temps l’existence du complexe actif et empêche sa persistance au cours de la mitose.
Actions chronologiques du complexe cycline A/CDK2
Phase S
En phase S, la cycline A associée à CDK2 devient le principal complexe kinase actif.
Le complexe cycline A/CDK2 ne se limite pas à soutenir la réplication, mais contribue à sa robustesse, à sa cohérence et à sa sécurisation tout au long de la phase S.
1. Elle assure une activation stable de CDK2, qui phosphoryle de nombreux facteurs de la réplication, notamment Cdc6, les complexes MCM, Treslin et plusieurs facteurs de la machinerie d’initiation et d’élongation.
Cette activité empêche le re-licensing des origines déjà engagées, en inhibant le rechargement des complexes de licensing, ce qui garantit qu’un segment d’ADN ne soit répliqué qu’une seule fois par cycle.
2. Elle participe également à la coordination entre la progression des fourches de réplication et les systèmes de surveillance, en maintenant une compatibilité fonctionnelle avec la signalisation ATR/Chk1 lors d’un stress réplicatif modéré.
Passage S ➞ G2 et transition vers CDK1
À mesure que la cellule progresse vers la fin de la phase S, l’activité cycline A/CDK2 décroît progressivement au profit d’une activité croissante du complexe cycline A/CDK1.
1. Ce basculement ne résulte pas d’un changement intrinsèque de la cycline A, mais d’une modification progressive du contexte cellulaire :
- En phase G2, la disponibilité fonctionnelle de CDK1 augmente sous l’effet de la levée progressive de l’inhibition exercée par Wee1 et Myt1 et l'activation de Cdc25 par leur phosphorylation par Plk1.
- La déphosphorylation partielle de CDK1 par Cdc25 permet alors la formation de complexes cycline A/CDK1 catalytiquement actifs, qui prennent progressivement le relais des complexes cycline A/CDK2.
2. Cette transition fonctionnelle initie une préparation moléculaire progressive de la cellule à l’entrée en mitose, affectant à la fois les structures nucléaires et l’organisation cytoplasmique.
a. Elle se traduit notamment par l’amorce de phosphorylations de substrats pré-mitotiques par CDK1, engageant des réorganisations nucléaires progressives, telles que :
- NPM1 contribuant à la désorganisation progressive du nucléole et aux réorganisations nucléaires précédant la prophase,
- des sous-unités de la condensine II, notamment CAP-H2, favorisant la préparation progressive de la condensation chromatinienne,
- certaines histones, H1 et H3, participant aux modifications structurales précoces de la chromatine.
b. Elle s’accompagne également de l’engagement de processus préparatoires au remodelage du cytosquelette et des centrosomes, participant à la maturation du fuseau mitotique :
- activation progressive d’Aurora A aux centrosomes,
- phosphorylation de protéines centrosomales telles que CEP192 et PCNT (péricentrine), contribuant à la maturation centrosomale et à la préparation de la bipolarité du fuseau.
2. La cycline A agit ainsi comme un facteur de continuité entre la logique réplicative et la logique mitotique, préparant le terrain pour l’activation brutale ultérieure du complexe cycline B/CDK1 (MPF).
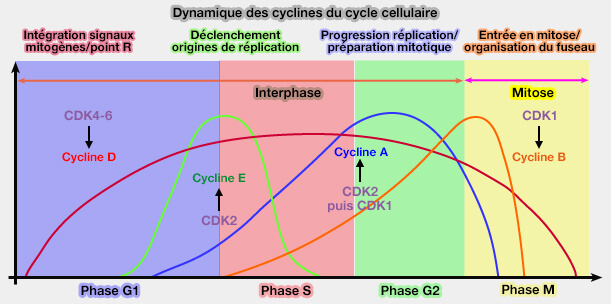
(Figure : vetopsy.fr)
Dégradation en prophase
Contrairement à la cycline B, la cycline A est détruite précocement au cours de la mitose sous le contrôle de l’APC/CCdc20.

Cette élimination constitue un événement fonctionnel majeur car elle met fin au programme préparatoire porté par la cycline A et transfère le contrôle de la mitose au complexe cycline B/CDK1 (MPF), qui assure alors la progression complète de la prophase à la télophase.
Remarque : une dérégulation de l’expression ou de l’activité de la cycline A est associée à plusieurs contextes pathologiques.
Sa surexpression favorise une accélération inappropriée de la phase S, une instabilité des programmes de réplication et une augmentation du stress réplicatif, contribuant à l’instabilité chromosomique observée dans de nombreux carcinomes et lymphomes.
Retour aux cyclines
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


