Transport des lipides
Lipoprotéines : HDL (lipoprotéines de haute densité)
Biogenèse
des HDL : formation des préβ-HDL
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Composés organiques
- Protides
- Acides nucléiques
- Glucides
- Lipides
- Vue d'ensemble des lipides
- Acides gras
- Classification des lipides
- Cholestérol
- Glycérides
- Trafic non vésiculaire des lipides et LTP
- Digestion et absorption entérocytaire des lipides
- Lipoprotéines
- Gouttelettes lipidiques
- Coenzymes
- Hormones
- Composés inorganiques
- Composés organiques
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Le début de la biogenèse des HDL (lipoprotéines de haute densité) est un processus complexe encore mal compris qui implique ABCA1 et apoA-I.
(Figure : vetopsy.fr)
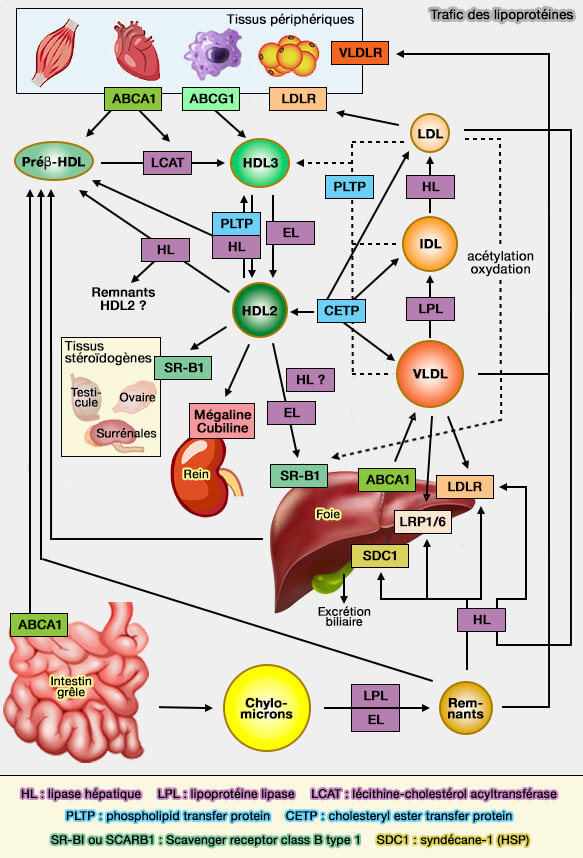
Vue d'ensemble de la biogenèse des HDL
1. La formation des HDL (lipoprotéines de haute densité) et leur métabolisme est un processus complexe encore mal compris qui implique le transfert de lipides cellulaires par ABCA1, transporteur ABC, vers une apoA-I extracellulaire pauvre en lipides pour génèrer des complexes lipide-apoA-I appelés particules HDL naissantes.
Ce processus, qui comprend plus de neuf modèles différents (Molecular mechanisms for ABCA1-mediated cholesterol efflux 2022), passe par plusieurs étapes :
- la formation des particules préβ-HDL qui comprend, selon les auteurs, les apoA-I peu lipidées et les HDL discoïdales,
- la formation des particules α-HDL sphériques.
Les mutations de l'apoA-I., ABCA1 et LCAT empêchent la formation de HDL contenant de l'apoA-I.
2. L'apoE et l'apoA-IV peuvent également synthétiser des particules HDL par le même processus (ApoA-IV promotes the biogenesis of apoA-IV-containing HDL particles with the participation of ABCA1 and LCAT 2013 et Pathway of biogenesis of apolipoprotein E-containing HDL in vivo with the participation of ABCA1 and LCAT 2007).
Formation des préβ-HDL
Les préβ-HDL discoïdales, appelées quelquefois α4-HDL après l'intervention de ABCA1, sont dépourvues de cœur lipidique.
Formation de novo
(Figure : vetopsy.fr)
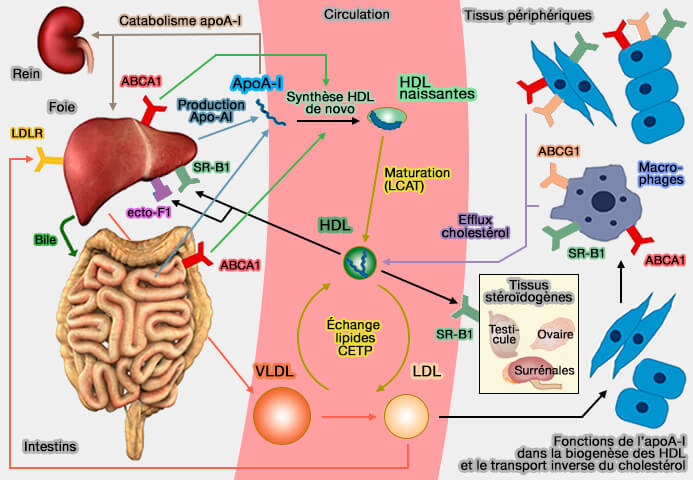
Synthèse de l'apoA-I
1. La première étape de la biogenèse des préβ-HDL est la synthèse de l'apoA-I :
- dans les hépatocytes pour la plus grande partie (75%),
- mais aussi dans les entérocytes (25%).

L'apoA-I est étudiée dans un chapitre spécifique.
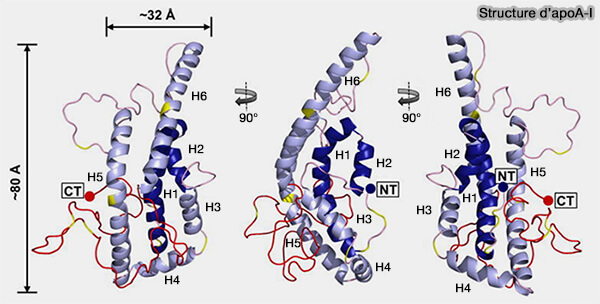
(Figure : vetopsy.fr d'après Melchior et coll)
2. L’apoA-I est synthétisé dans le réticulum endoplasmique (RE) et serait sécrétée sous forme de monomères libres dans la ciculation.
3. L'apoA-I acquérerait rapidement certains phospholipides (PL), ce qui déclencherait sa dimérisation et la formation de très petites particules discoïdes de préβ1-HDL sans avoir recours à ABCA1 (High-density lipoprotein subpopulation profiles in lipoprotein lipase and hepatic lipase deficiency 2016).
Une minorité de particules préβ1 formerait de plus grands disques contenant 3 à 5 apoA-I et seulement une petite quantité de lipides (agrégats d'apoA-I).
-
Remarque : on distigue dans les préβ-HDL,comme d'ailleurs dans les α-HDL, des LpAI contenant uniquement de l'apoA-I et les LpAI:AII contenant apoA-I et apoA-II (
rôle de l'apoA-II dasn la formation des HDL).
Intervention d'ABCA1
L'étape limitante de la formation de HDL nécessite ABCA1 (ATP-Binding Cassette transporter A1), transporteur ABC, qui crée un microdomaine au niveau de la membrane plasmique pour former des HDL-C, HDL naissantes discoïdales contenant du cholestérol libre (FC) et des phospholipides (PL).
Cette transformation permet de produire des α4-HDL, i.e. 7,4 nm, qui sont discoïdales et non sphériques comme les autres α-particules.
- Ces α4-HDL comprendrait deux molécules d'apoA-I (
apoA-I dans les HDL naissantes).
- Toutefois, on peut trouver des HDL discoïdales plus grandes contenant 3 à 5 molécules d'apoA-I à demi-vie très courtes qui peuvent être détectées chez les sujets déficients en LCAT (Role of LCAT in HDL remodeling: investigation of LCAT deficiency states 2007).

L'ABCA1 est étudié dans un chapitre spécifique.
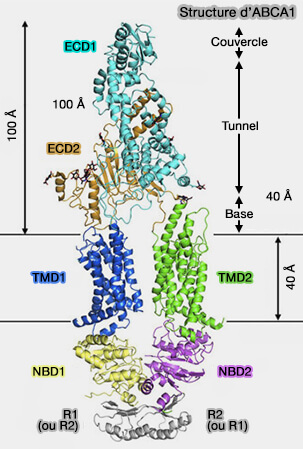
(Figure : vetopsy.fr d'après Philips)
1. ABCA1 est une protéine ubiquitaire qui se trouve dans :
- les hépatocytes, sur leur surface basolatérale,
- les entérocytes (Intestinal ABCA1 directly contributes to HDL biogenesis in vivo 2006).
- les macrophages (Apolipoprotein A-I but not high-density lipoproteins are internalised by RAW macrophages: roles of ATP-binding cassette transporter A1 and scavenger receptor BI 2008),
- les cellules endothéliales (Carboxyl Terminus of Apolipoprotein A-I (ApoA-I) Is Necessary for the Transport of Lipid-free ApoA-I but Not Prelipidated ApoA-I Particles through Aortic Endothelial Cells 2011).
- le cerveau et divers autres tissus.
2. ABCA1 favorise l'efflux des phospholipides cellulaires (PL) et et du cholestérol vers les apoA-I peu lipidés ou vers d'autres apolipoprotéines, comme l'apoE et l'apoA-IV, mais pas vers les particules HDL sphériques (Reverse Cholesterol Transport: Molecular Mechanisms and the Non-medical Approach to Enhance HDL Cholesterol 2019).
Cela génère des HDL naissants, un fragment bicouche formé de 200 à 700 lipides enveloppés par deux à quatre molécules d'apoA-I.
Remarque : les mutations du gène ABCA1 à l'origine de la maladie de Tangier sont associées à des taux plasmatiques extrêmement faibles de HDL-C, une caractéristique de la maladie (Tangier desease 2023).
3. Neuf modèles différents de biogenèse des HDL sont connus sans qu'il y ait un consensus (Molecular mechanisms for ABCA1-mediated cholesterol efflux 2022).
a. Toutefois, deux points semblent acquis.
- ABCA1 transloque à la fois les phospholipides (PL) et le cholestérol des membranes plasmiques vers l'ECD d'ABCA1 (Unraveling the complexities of the HDL lipidome 2013).
- Les extrémités C-terminales et N-terminales de l'apoA-I sont essentielles à la formation des HDL.
b. Deux grandes catégories de modèles ont été proposés pour expliquer comment se forment les particules HDL-C naissantes (
- Selon le modèle de chargement dit direct, ABCA1 transfère directement les lipides à l'apoA-I pendant qu'elle est liée au transporteur.
- Dans le modèle dit indirect, l'activité de translocation des phospholipides de la protéine ABCA1 forme des domaines membranaires spécifiques et l'ApoA-I acquiert des lipides à travers ces domaines.
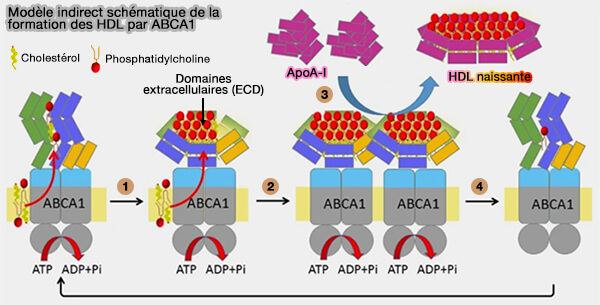
(Figure : vetopsy.fr d'après Ishigami et coll)
Remarque : certains auteurs distinguent souvent la formation des particules préβ-HDL qui correspondent aux apoA-I peu lipidées des HDL discoïdales qui contiennent plus de lipides.
Dans ce cas, les particules préβ-HDL, s'enrichissent progressivement en cholestérol pour former des particules discoïdes.
Formation par remodelage des HDL
1. Des particules préβ-HDL peuvent être aussi créées, i.e. mais pas de novo, par remodelage d'HDL matures, en raison de l'action combinée de (High-density lipoprotein subpopulation profiles in lipoprotein lipase and hepatic lipase deficiency 2016) :
- CETP (Cholesteryl Ester Transfer Protein),
- PLTP (Phospholipid transfer protein),
- HL (Hepatic Lipase),
- SR-BI (Scavenger Receptor-class B1).
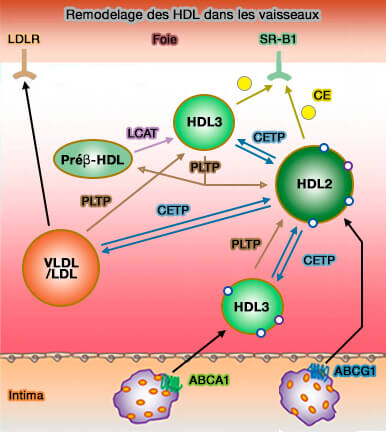
(Figure : vetopsy.fr d'après Oulmet et coll)
En effet, les HDL sont facilement perturbées par des perturbations physico-chimiques, mais aussi par les molécules précédentes, qui peuvent dissocier l'apoA-I des HDL, pour laisser que les liipdes avec l'apoA-II.
2. Elles peuvent aussi provenir par des voies détounées des TRL (lipoprotéines riches en triglycérides), i.e. chylomicrons ou VLDL (lipoprotéines de très basse densité) après hydrolyse des triglycérides par la LPL (LipoProtéine Lipase), avec un effet permissif de la PLTP.
La LPL diminue la taille du cœur hydrophobe de ces particules et les composés de surface libérés dans le sang, pourrait forment les préβ-HDL ou enrichissent les α-HDL pour augmenter leur taille.
3. Les préβ-HDL pourrait aussi accepter le cholestérol par diffusion passive, selon son gradient de concentration, de la membrane plasmique vers le milieu extracellulaire, pour être intégré à la surface des lipoprotéines circulantes.
Remarque : le transporteur ABCG1 (Adenosine triphosphate-Binding Cassette transporter G1) est directement impliqué dans l’efflux du cholestérol de plusieurs tissus vers les HDL2 et HDL3, mais pas aux préβ-HDL.
Formation des α-HDL sphériques
Les préβ-HDL discoïdales, dépourvues de cœur lipidique, se transforment en α-HDL sphériques, contenant un noyau hydrophobe sous l'action de la LCAT dont le principal activateur est l'apoA-I.
BiochimieChimie organiqueBioénergétiqueProtidesGlucidesLipidesAcides grasPhospholipidesPhosphoinositidesCholestérolAcides biliairesGlycéridesDigestion et absorption entérocytaire des lipidesLipoprotéinesApolipoprotéinesTrafic des lipoprotéinesRécepteurs des lipoprotéinesGouttelettes lipidiques (LD)EnzymesCoenzymesVitaminesHormonesComposés inorganiquesTransport membranaireMoteurs moléculairesVoies de signalisation


