Lipides
Acide gras
Synthèse des acides gras
cytoplasmiques
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Composés organiques
- Protides
- Acides nucléiques
- Glucides
- Lipides
- Vue d'ensemble des lipides
- acides gras (FA)
- Classification des lipides
- Cholestérol
- Glycérides
- Trafic non vésiculaire des lipides et LTP
- Digestion et absorption entérocytaire des lipides
- Lipoprotéines
- Gouttelettes lipidiques (LD)
- Coenzymes
- Hormones
- Composés inorganiques
- Composés organiques
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

La synthèse des acides gras (FA) dans le cytoplasme nécessite de l'acétyl-CoA et du NADPH grâce à FAS I (Fatty Acid Synthase ou acide gras synthase).
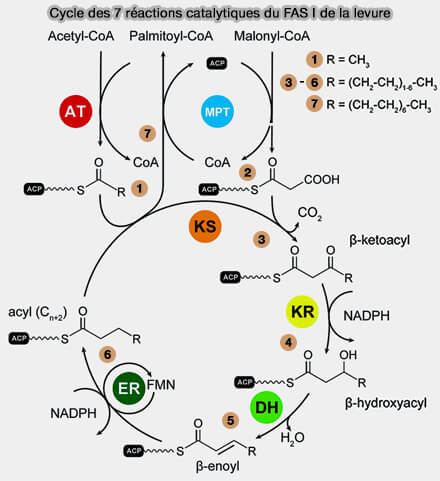
Étapes de la voie cytoplasmique (voie de Wakil)
La biosynthèse des acides gras pairs s'effectue par additions successives de fragments à 2 atomes de carbone pour atteindre 16 carbones, i.e. l'acide palmitique (16:0), i.e. palmitate chez les mammifères et le palmitoyl-CoA chez la levure
Dans vetopsy.fr, nous la représenterons en sept étapes.
- Les deux premières correspondent à des étapes d'initiation de la synthèse.
- Les autres étapes, i.e. 3 à 6, sont des étapes de la synthèse proprement dite.
- La 7ème étape est la libération de la FAS.

Les deux groupes thiol, $\ce{R-S-H}$, i.e. de l'ACP et de KS sont essentiels à la prise en charge des groupes acyles ($\ce{R-C(=O)-R'}$).
1ère étape : formation d'acétyl-ACP
Le groupe acétyle $\ce{CH3-CO-}$) est transféré à partir de l'acyl-CoA sur l'ACP (Acyl Carrier Protein), i.e. il forme le dernier groupe des acides gras formés.
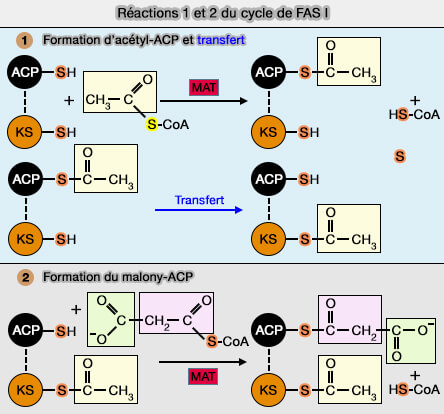
(Figure : vetopsy.fr d'après Herbst et coll)
1. La formation d'acétyl-ACP est catalysé par le domaine MAT (Malonyl/AcétylTransférase), i.e. l'acétyl-CoA:[ACP] S-acétyltransférase, (EC 2.3.1.38).
$\ce{CH3-CO-S-CoA + S-ACP}$
$\leftrightharpoons$
$\ce{HS-CoA + CH3-CO-S-ACP}$
2. Le groupe acyle quitte le groupe SH de l'ACP et migre sur le groupe SH du domaine KS (Kéto-acylSynthase).
2ème étape : formation
de malonyl-ACP
Suite à la première étape, le groupe SH de l'ACP est alors disponible pour accepter un reste malonyl apporté également par l'acyl-CoA, réaction catalysée par la MAT (Malonyl/AcétylTtansférase), i.e manolyl-CoA:[ACP] S-acétyltransférase (EC 2.3.1.39).
$\ce{HOOC-CH2-CO-S-CoA + S-ACP}$ $\leftrightharpoons$ $\ce{HS-CoA + HOOC-CH2-CO-S-ACP}$
Le malonyl-CoA se forme è partir de l'acétyl-CoA (
3ème étape : formation de l'acétoacétyl-ACP par condensation
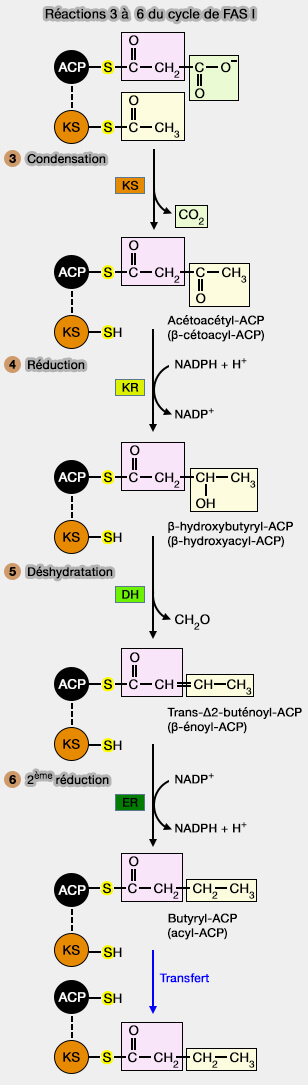
(Figure : vetopsy.fr d'après Herbst et coll)
L'acétoacétyl-ACP est formé par la condensation des restes acétyle et malonyle fixés au complexe enzymatique.
1. Le groupe acétyle est transféré du SH du domaine KS au malonyl groupe du SH de l'ACP formant un groupe méthyl N-terminal.
2. La réaction catalysée par le domaine KS (Kéto-acylSynthase), i.e les enzymes sont souvent appelées KAS, ou β-cétoacyl-ACP synthase (EC 2.3.1.41) implique une décarboxylation, i.e. donnant une réactivité particulière au groupe méthylène en C-2, le rendant capable de réagir avec le carboxyle du groupe acétyle.
$\ce{CH3-CO-S-ACP + HOOC-CH2-CO-S-ACP}$
$\leftrightharpoons$
$\ce{CH3-CO-CH2-CO-S-ACP + CO2}$
a. Les β-cétoacyl-ACP synthases sont aussi appelées 3-cétoacyl-ACP synthases, en anglais ketoacyl-ACP synthases.
b. Les β-cétoacyl-ACP synthases sont classées en plusieurs groupes et on trouve des incohérences dans les articles (3-Ketoacyl-ACP synthase (KAS) III homologues and their roles in natural product biosynthesis 2019).
4ème étape : réduction
de l'acétoacétyl-ACP
L'acétoacétyl-ACP subit une réduction sur C3 pour former le β-hydroxybutyryl-ACP, réaction catalysée par le domaine KR (Keto-acylRéductase), i.e les enzymes sont souvent appelées KAR, bêta-cétoacyl-ACP réductase I (EC 1.1.1.100).
$\ce{CH3-CO-CH2-CO-S-ACP + NADPH + H+}$ $\leftrightharpoons$ $\ce{CH3-CHOH-CH2-CO-S-ACP + NADP+}$
5ème étape : déshydratation
de l'alcool secondaire
L'alcool secondaire sur C2 est déhydraté, réaction catalysée par le domaine DH (DésHydratase), i.e. 3-Hydroxyacyl ACP dehydratase (EC 4.2.1.59).
$\ce{CH3-CHOH-CH2-CO-S-ACP}$ $\leftrightharpoons$ $\ce{CH3-CH=CH2-CO-S-ACP + H2O}$
6ème étape : deuxième réduction
1. La deuxième réduction est catalysée par le domaine ER (Enoyl Réductase), i.e. énoyl-ACP reductase (EC 1.3.1.39), aboutissant à un reste butyryl-ACP, i.e. butyryl correspondant à l'acide butyrique ou butanoïque à 4 atomes de carbone
$\ce{CH3-CH=CH2-CO-S-ACP + NADP+}$ $\leftrightharpoons$ $\ce{CH3-CH2-CH2-CO-S-ACP + NADPH}$
2. La réaction implique le transfert du reste butyryle du SH de l'ACP sur le SH du KS, i.e. le SH central de l'ACP pourra alors fixer un nouveau reste malonyle.

Les 5 réactions, i.e. 2 à 6, forment un cycle qui se répète et qui permet à chaque fois l’allongement de la chaine de deux carbones supplémentaires pour aboutir au palmitate ou plutôt le palmityl-ACP en C16.
Remarque : La palmityl-ACP pourrait être directement incorporable dans les glycérides et les phospholipides (PL).
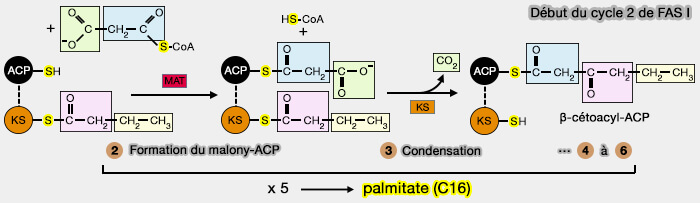
(Figure : vetopsy.fr)
7ème étape : libération de l'acyl-ACP ou de l'ACP
Une 7ème étape qui permet permettre la libération du SH du domaine ACP est variable suivant les règnes.
1. Chez les végétaux et les animaux, le dernier stade correspond à la libération de l'ACP et de palmitate par une oleoyl-ACP hydrolase (EC 3.1.2.14).
$\ce{palmityl-S-ACP + H2O}$ $\leftrightharpoons$ $\ce{HS-ACP + palmitate}$
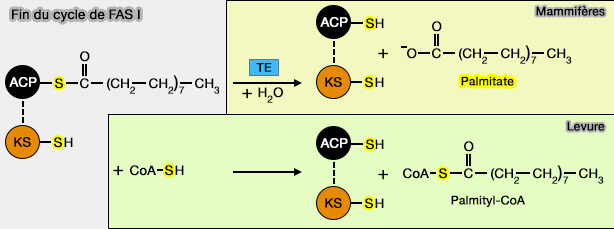
(Figure : vetopsy.fr)
2. Chez la levure, le dernier stade correspond à la libération de l'acyl-ACP qui libère le thiol central.
$\ce{palmityl-S-ACP + HS-COA}$ $\leftrightharpoons$ $\ce{HS-ACP + palmitoyl-CoA}$
Bilan de la biosynhèse
1. Le bilan global chez la levure est :
$\ce{Acétyl-CoA + 7 malonyl-CoA + 14 NADPH + 14 H+}$ $\leftrightharpoons$ $\ce{palmitoyl-CoA + 7 CoA + 7 H2O + 14 NADP+ + 7 CO2}$
(Figure : vetopsy.fr d'après Herbst et coll)
2. Chez les végétaux et les animaux, l'acide palmitique est libre ce qui entraîne la récupération de 8 CoA au lieu de 7 et 6 H2O au lieu de 7, une est utilisé dans la libération du palmitate.
$\ce{Acétyl-CoA + 7 malonyl-CoA
+ 14 NADPH + 14 H+}$
$\leftrightharpoons$
$\ce{palmitate + 7 CoA + 6 H2O + 14 NADP+ + 7 CO2}$
Si on ajoute le bilan de la synthèse de malonyl-CoA :
$\ce{7 Acétyl-CoA + 7 CO2 + 7 ATP}$ $\leftrightharpoons$ $\ce{7 malonyl-CoA + 7 ADP + 7 Pi}$
On obtient :
$\ce{8 Acétyl-CoA + 7 ATP + 14 NADPH + 14H+}$ $\leftrightharpoons$ $\ce{palmitate + 8 CoA + 6 H2O + 14 NADP+ + 7 ADP + 7 Pi}$
Biosynthèse des acides gras impairs
Dans le cas des acides gras à nombre impair de carbone, c'est le propionyl-CoA qui remplace l'acétyl-CoA (Microbial production of odd‐chain fatty acids 2012 et Metabolism of Odd-numbered Fatty Acids and Even-numbered Fatty Acids in Mouse 2008).
Le propionyl-CoA est transformé est transformé en 3-oxovaléryl-ACP, puis suit les réactions du cycle cytoplasmique classique.
$\ce{CH3-CH3-CO-S-ACP + HOOC-CH2-CO-S-ACP }$
$\leftrightharpoons$
$\ce{CH3-CH3-CO-CH2-CO-S-ACP + CO2}$

Les sources de propionyl-CoA et son métabolisme sont traités dans la régulation du cycle de Krebs.
Sources des molécules des réactions
BiochimieChimie organiqueBioénergétiqueProtidesGlucidesLipidesAcides grasSynthèse des acides grasβ-oxydationCorps cétoniquesOxylipinesLipides vraisLipides vrais simplesLipides vrais complexesLipoïdesCholestérolGlycéridesPhospholipidesGlycérophospholipidesSphingophospholipidesTrafic non vésiculaire et LTPDigestion et absorption entérocytaire des lipidesLipoprotéinesApolipoprotéinesGouttelettes lipidiques (LD)EnzymesCoenzymesVitaminesHormonesComposés inorganiquesTransport membranaireMoteurs moléculairesVoies de signalisation


