Endocrinologie : hormones hypothalamiques
GnRH : régulation de la sécrétion par des facteurs internes
- Endocrinologie
- Système hypothalamo-hypophysaire
- Neurosécrétion
- Système hypothalamo-neurohypophysaire
- Système tubéro-infundibulaire
- Hormones du système hypothalamo-hypophysaire
- Hormones hypohysaires
- Hormones à visée reproductive
- selon leur lieu de production
- selon leur structure

La GnRH (Gonadotropin Releasing Hormone ou gonadolibérine) est une hormone hypothalamique peptidique stimulant la synthèse et la sécrétion de la LH et de la FSH et par l'adénohypophyse.
- La GnRH est synthétisé par les neurones hypothalamiques, d'où le nom de neurohormone.
- Elle est encore appelée LH-RH (Luteinizing Hormone Releasing Hormone).
La sécrétion de la GnRH est modulée par de nombreux stimuli externes et internes.
Régulations de la sécrétion
de GnRH par des stimuli internes
Puberté

La puberté est provoquée par l'augmentation de la fréquence et de l'intensité des pulses de GnRH (puberté et pulses de GnRH)
Les pulses de GnRH sont présents pendant la période foetale et subissent, pendant l'enfance, une inhibition du système nerveux central jusqu'à la puberté, vraisemblablement par le GABA.
Le mécanisme est mal connu et il semble que le glutamate, à cette période, augmente son activité pour déclencher les pulses de GnRH.
Le système kisspeptine/GPR54 est impliqué dans ce processus car l'altération du récepteur GPR54 maintient les individus à un stade pré-pubertaire.
Stéroïdes circulants
Les stimuli internes, les plus importants dans des conditions " normales ", sont essentiellement le taux des stéroïdes circulants.
Chez la femelle
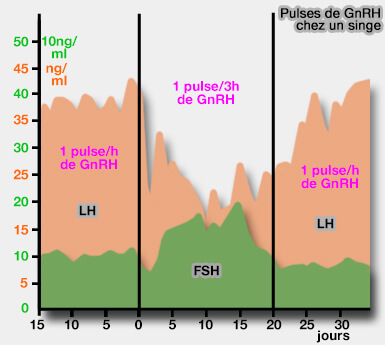
en fonction des pulses de GnRH
(Figure : vetopsy.fr)
Chez la femelle (dans le cas décrit chez la femme), la fréquence et l'amplitude des pulses de GnRH varient au cours des cycles ovariens.
1. Au début de la phase folliculaire, lorsque le taux d'oestrogènes est bas, les pulses de GnRH ont lieu toutes les 2-3 heures environ.
2. Au cours de la phase folliculaire et la phase ovulatoire, lorsque le taux des oestrogènes est élevé, cette fréquence passe à un pulse toutes les heures.
3. Au cours de la phase lutéale, lorsque le taux de progestérone est élevé, la fréquence diminue à un pulse toutes les 4 heures.
Chez le mâle

La testostérone inhibe la sécrétion hypothalamique de GnRH et la sécrétion hypophysaire de LH. Ainsi la testostéronémie est maintenue constante : c'est un exemple d'homéostasie.
Chez le mâle, les pulses de GnRH sont constants et ont lieu toutes les 60 à 90 minutes.
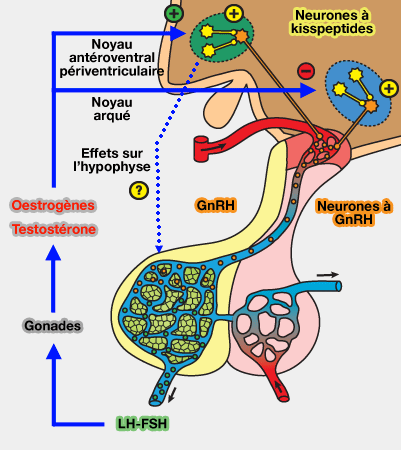
les neurones à GnRH via les kisspeptines
(Figure : vetopsy.fr)
Le taux de testostérone dans le sang est détecté
en permanence par le complexe hypothalamo-hypophysaire par la concentration en oestrogènes (
- Lorsque le taux est bas, la sécrétion de la GnRH augmente.
- Lorsque le taux est élevé, elle diminue.
Kisspectines
et régulation

Les neurones sécréteurs de GnRH n'expriment pas le récepteur aux oestrogènes (ERα). Il faut donc que le rétrocontrôle passe par des interneurones sensibles aux stéroïdes.
Vue d'ensemble
1. La découverte récente du rôle essentiel du système kisspeptine/GPR54 dans la régulation de l’axe gonadotrope a révolutionné le domaine de la biologie de la reproduction.
- Les kisspeptines (KP) ont d'abord été découvertes en 1996 : le gène KiSS-1 produit une protéine qui supprime les métastases des mélanomes (KP54 : 54 aa).
- Puis, on a trouvé une KP14, 13 et 10, sécrétées par le placenta (Mechanistic insights into the more potent effect of KP-54 compared to KP-10 in vivo 2017).
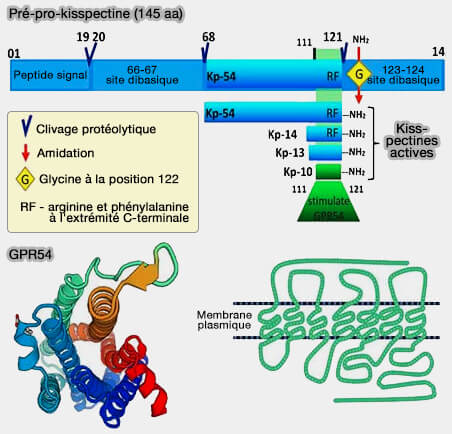
(Figure : vetopsy.fr d'après Trevisan et coll)
2. Les kisspeptines sont les ligands d'un récepteur couplé à une protéine Gq/11 (GPR54) s'exprimant à la surface des neurones à GnRH dans l'aire préoptique et le noyau arqué (Kisspeptin/GPR54 System: What Do We Know About Its Role in Human Reproduction? 2018).
Lorsque la kisspeptine stimule son récepteur, le Gq/11 active la phospholipase C (PLCβ) qui hydrolyse le phosphatidylionositol 4,5-bisphosphate (PIP2) produisant des seconds messagers.
- L'inositol 1,4,5-trisphospate (IP3) et le diacylglycérol (DAG) stimule le réticulum endoplasmique (RE) pour mobiliser le calcium (Ca++). L'augmentation des niveaux intracellulaires de Ca++ active les voies de signalisation dépendantes du calcium dans les neurones à GnRH.
- Le DAG active la protéine kinase C dépendante du calcium (PKC) qui active les kinases 1 et 2 régulées par le signal extracellulaire (ERK1 et ERK2).
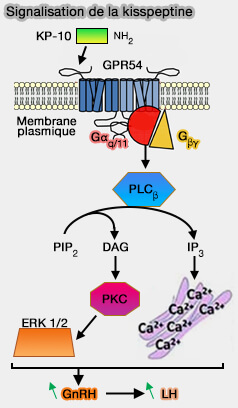
(Figure : vetopsy.fr
d'après Trevisan et coll)
3. Les mutations du récepteur GPR54 (PR54 contient 396 acides aminés avec une homologie de 45% avec les domaines transmembranaires des récepteurs de la galanine) ou les souris KO pour ce gène provoquent des anomalies dans le système reproducteur.
- Les humains et les souris ne deviennent pas pubères, souffrent d'un hypogonadisme (concentrations d'oestrogènes, de testostérone, de FSH et de LH basses), sont pourvus de gonades de petite taille et sont stériles.
- Par contre, le taux de GnRH cérébral est normal : c'est donc sa libération qui est perturbée, et non sa synthèse.

L'administration de kisspeptine, quelque soit la voie, provoque une libération massive de GnRH qui stimule les gonatrophines (FSH et LH), quelle que soit l'espèce.
- La kisspeptine est le plus puissant stimulateur de la GnRH.
Rétrocontrôles
Le dimorphisme sexuel cérébral est patent pour les neurones à kisspeptines :
- Chez la femelle, le noyau arqué et le noyau antéroventral périventriculaire contiennent autant de neurones à kisspeptines.
- Chez le mâle, le noyau périventriculaire en contient peu.
Les neurones à kisspeptine expriment fortement le récepteur aux oestrogènes (ERα).
Que se passe-t-il pendant le cycle ovarien ?
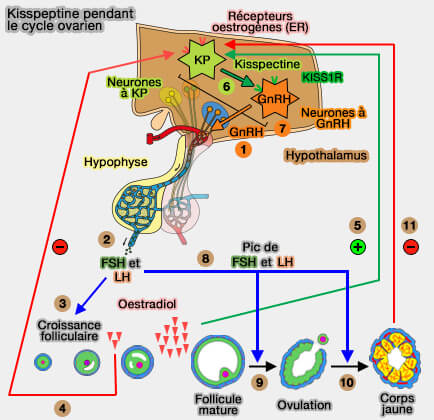
(Figure : vetopsy.fr d'après Trevisan et coll)
1. La GnRH stimule l'antéypophyse.
2.
Cette stimulation libère la FSH et la LH.
3.
Ces hormones stimulent la croissance folliculaire et les follicules commencent à produire de l'oestradiol.
4.
L'œstradiol supprime l'activation de l'axe hypothalamo-hypophyso-gonadique.
5.
À la fin de la phase folliculaire, lorsque le follicule principal devient dominant et atteint environ 12 mm, le niveau d'oestradiol augmente et stimule les récepteurs à l'oestradiol (ER) des neurones à kisspeptine (Kp) pour libérer la kisspeptine.
6.
Les neurones Kp stimulent les neurones à GnRH.
7.
La GnRH stimule l'hypophyse.
8.
Cette stimulation provoque le pic de LH (et de FSH).
9. L'ovulation se produit.
10. Le corps jaune se développe.
11.
Le corps jaune inhibe l'axe hypothalamo-hypophyso-gonadique par la production de :
- la progestérone,
- l'oestradiol,
- l'inhibine A.
Il semblerait que les neurones à kisspeptine :
- du noyau arqué interviennent dans les rétrocontrôles négatifs des stéroïdes sexuels,
- du noyau antéroventral périventriculaire interviennent dans les rétrocontrôles positifs des stéroïdes sexuels.
Autres facteurs
La sécrétion de GnRH est modulée par de nombreux neuropeptides.
Toutefois, les cellules hypothalamiques expriment peu de récepteurs neuropeptidiques à leur surface ! D'autres voies de régulation ont été explorées.
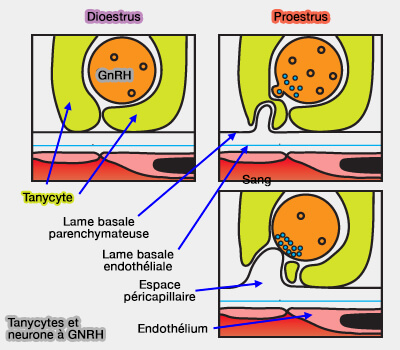
(Figure : vetopsy.fr d'après Prévot)
1. Les terminaisons nerveuses à GnRH ne sont pas simplement des synapses neuro-hémales comme la plupart des autres neurohormones, mais englobées dans des tanycytes , i.e. cellules épendymaires de l'éminence médiane ( 
- Ces cellules gliales contrôleraient la libération de GnRH tout, en modulant l'accès des terminaisons nerveuses aux capillaires via de nombreuses substances (
interactions avec les cellules gliales).
- De plus, les tanycytes peuvent changer de forme selon l'état hormonal et peuvent séparer les terminaisons axonales des capillaires du système porte : les terminaisons nerveuses étaient observées au contact des capillaires ou en étaient séparés par des prolongements gliaux selon l'état stéroïdien des animaux. Des jonctions neuro-hémales ne sont visibles que le jour du prooestrus au moment où l'on observe le pic de GnRH dans le sang porte (
tanycytes et sécrétions de GnRh).
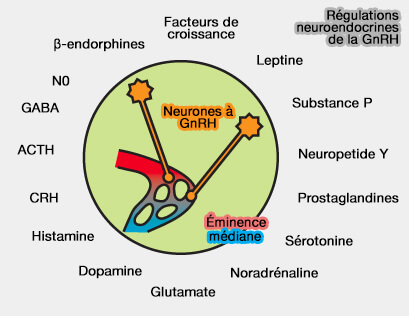
(Figure : vetopsy.fr)
Le monoxyde d'azote (NO), d'origine endothéliale, modifie le cytosquelette d'actine des tanycytes et favorise l'accès des terminaisons nerveuses aux capillaires le jour du prooestrus (taux de GnRH maximal).
2. De nombreux autres facteurs (en particulier des neurotransmetteurs) modulent la sécrétion de GNRH :
- freinateurs comme le GABA, certains opioïdes endogènes, la dopamine, les prostaglandines ;
- excitateurs comme le glutamate, la noradrénaline, la sérotonine, mais également, les facteurs de croissances (TGF, EGF), l'AMP cyclique ;
- variables comme le neuropeptide Y suivant le taux d'oestradiol…
Lors de la lactation par exemple, la fréquence des tétées, qui déclenchent une sécrétion de β-endorphines dans le système nerveux central, réduit les pulses de GnRH.

C'est pourquoi aussi que, de nombreux états pathologiques, qu'ils soient somatiques ou comportementaux (ainsi que la chimiothérapie les combattant), provoquent une baisse de l'activité hormonale gonadique.
- le stress qui, par sa stimulation de la synthèse des corticoïdes, inhibe les sécrétions hypothalamiques,
- les phénomènes immunologiques (infections…).


