Enzymes
Effecteurs des réactions enzymatiques
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Un effecteur, en bioénergétique, est un composé chimique très varié qui intervient dans les réactions enzymatiques soit pour les activer, soit, au contraire, pour les inhiber.
Activateurs

Un activateur est une substance qui a pour effet d'augmenter la vitesse d'une réaction enzymatique.
Inhibiteurs

Un inhibiteur est une substance qui a pour effet de diminuer la vitesse d'une réaction enzymatique.
(Figure : vetopsy.fr d'après Thomas Shafee)
Dans cette partie générale, on ne parlera que de l'apoenzyme.
1. L'enzyme doit reconnaître son substrat, s'y combiner transitoirement et le transformer.
- La combinaison enzyme/substrat est un complexe stéréospécifique formé grâce à des liaisons faibles, non covalentes, qui ne peuvent s'engager qu'en raison d'une complémentarité structurale.
- Dans certains cas, des liaisons covalentes se forment de façon transitoire à l'un ou plusieurs des stades de la réaction enzymatique.
2. Dans la plupart des cas, la molécule de protéine enzymatique est infiniment plus volumineuse que celle du substrat.
- Seul, le site actif, zone privilégiée de la protéine qui peut être constituée que de quelques résidus, intervient réellement dans la réaction.
- Ces résidus peuvent être très éloignés les uns des autres dans la structure primaire de la protéine, mais se trouvent rapprochés dans l'espace grâce aux repliements de la structure de l'enzyme.
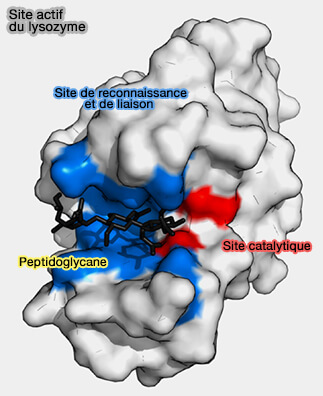
Site actif
Le site actif comporte deux sites voisins :
- le site de reconnaissance, site de fixation du substrat,
- le site catalytique, site responsable de la réalisation de la réaction chimique catalysée.
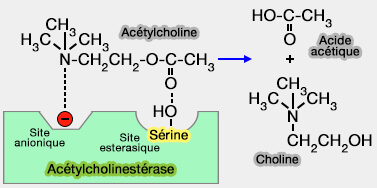
Soit la cholinestérase, cette enzyme, qui se combine à l'acétylcholine pour l'hydrolyser, possède :
- un site anionique chargé négativement, qui reconnaît et fixe la partie du substrat à charge positive,
- un site " estérasique " comportant deux groupes réactionnels : un hydroxyle électrophile d'une sérine, un noyau imidazole nucléophile d'un résidu histidine, qui sont mis en jeu pour l'hydrolyse de la fonction ester.
(Figure : vetopsy.fr)
1. Le site actif d'une enzyme se trouve à l'intérieur de la molécule globulaire protéique, en général dans une sorte de gouttière, i.e. au sein d'un environnement hydrophobe où des échanges électroniques avec le substrat peuvent se réaliser facilement.
- Les quelques résidus impliqués directement dans la réaction enzymatique se trouvent, au niveau du site actif, au contact du substrat et sont, le plus souvent, hautement conservés.
- Des résidus jouent un rôle indirect en assurant la flexibilité de la structure tertiaire au voisinage du site actif.
- D'autres ne paraissent jouer aucun rôle et sont hautement variables.
2. Lors de la reconnaissance, des modifications conformationnelles de la protéine orientent, de manière optimale, les groupes catalytiques, pour optimiser la réaction.
3. Les enzymes agissent, de façon comparable à celle d'un catalyseur minéral, en abaissant l'énergie d'activation des molécules, permettant la réalisation de nombreuses réactions chimiques dans des conditions physiologiques.
Le facteur d'accélération par rapport à la réaction chimique sans catalyseur est de l'ordre d'une centaine de fois, et est dû à plusieurs facteurs.
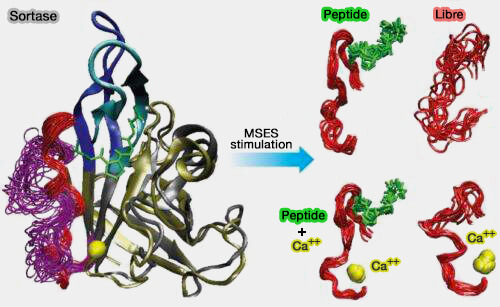
(Figure : vetopsy.fr d'après Kei Moritsugu)
Tout d'abord, il existe un effet de positionnement et de proximité entre la molécule et le site actif.
Ensuite, un effet de catalyse acide-base intervient.
- Aux pH habituels de fonctionnement des enzymes, les concentrations en $\ce{H-}$ et $\ce{0H-}$ sont trop faibles pour que leur participation soit déterminante, mais, en revanche, plusieurs acides aminés des protéines enzymatiques possèdent des groupes fonctionnels ionisables, carboxyliques ou aminés.
- Leur dissociation dépend du pH à l'extérieur de la molécule, mais ils sont peu dissociés lorsqu'ils sont au sein de l'environnement hydrophobe, comme c'est le cas au niveau du site actif.
- Les acides aspartique et glutamique, la lysine et l'histidine peuvent ainsi intervenir, et l'action hydrolysante du lysozyme sur les liaisons glycosidiques est expliquée par la mise en jeu de ces résidus.
Puis, un effet de contrainte conformationnelle est capable de jouer un rôle important dans le déclenchement de certaines réactions.
Enfin, un effet de catalyse covalente est fréquemment observé, comme dans la formation d'une base de Schiff ($\ce{R2C=NR' avec R' ≠ H}$), entre un substrat à groupe carbonyle ($\ce{C=O}$) et un groupe amine primaire ($\ce{NH2}$) du site actif, comme lors de l'hydrolyse d'un peptide par l'α-chymotrypsine.
Classification des enzymes
Biologie cellulaire et moléculaireConstituants de la celluleMatrice extracellulaireReproduction cellulaireBiochimieProtidesGlucidesLipidesEnzymesCoenzymesPeptidases/protéasesKinasesPhosphatasesGTPasesProtéines GPetites GTPasesATPasesPompesTransporteursHormonesTransport membranaireMoteurs moléculairesVoies de signalisation


