Trafic vésiculaire
Voie sécrétoire
Modèles du trafic réticulum/Golgi (EGT)
- En construction

De nombreux modèles différents et leurs combinaisons ont été proposés pour expliquer les données expérimentales sur le transport réticulum/Golgi (EGT).
À l'heure actuelle, quatre principaux modèles de transport intracellulaire reposant sur trois grands principes, i.e. dissociation, progression et diffusion, sont décrits :
- le modèle vésiculaire (VM),
- le modèle de maturation-progression des citernes (CMPM),
- le modèle de diffusion (DM),
- le modèle kiss-and-run (KARM), qui existe sous forme de deux variantes, symétrique et asymétrique.

Vous pouvez lire l'article qui a inspiré ce chapitre : Models of Intracellular Transport: Pros and Cons (2019).
Modèle vésiculaire (VM) de l'EGT
1. Le modèle vésiculaire (VM) de l'EGT (Endoplasmic reticulum Golgi Trafic ou trafic réticulum endoplasmique/Golgi) suppose que la sortie des cargos du réticulum endoplasmique (RE) se produit dans les bourgeons recouverts de COPII (
- Ces bourgeons subissent une fission pour former des vésicules sphériques recouvertes de manteau COPII.
- Après séparation de leur revêtement, ces vésicules sont transportées vers l'appareil de Golgi sous forme de vésicules individuelles ou d'agrégats de vésicules.

Les vésicules à manteau COPII sont étudiées dans un chapitre spécial.
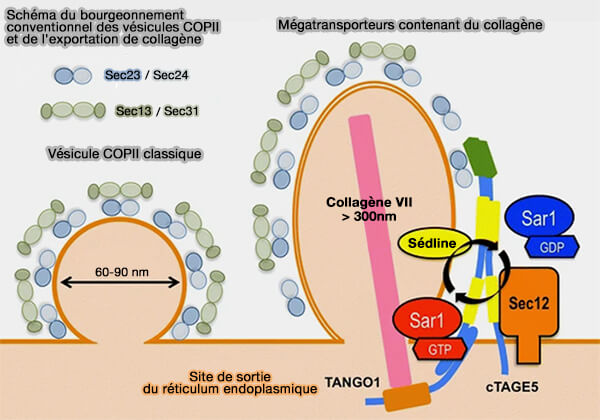
(Figure : vetopsy.fr d'après Saito et Katada)
Remarque : Tango1 intervient dans la sortie des mégacargos comme le procollagène et pourrait former des canaux qui relient le RE au Golgi (
1. COPII est important pour la sortie de plusieurs cargos du RE (Noncanonical autophagy at ER exit sites regulates procollagen turnover 2018).
- Le cargo se déplaçant du RE vers le Golgi passe par plusieurs étapes de colocalisation, i.e. COPII, COPII/COPI et COPI, pour finalement subir une centralisation.
- COPII concentre le cargo sur les membranes artificielles (Visualization of cargo concentration by COPII minimal machinery in a planar lipid membrane 2009).
- Les ERES (ER Exit Sites) sont des zones du réticulum endoplasmique (RE) spécialisées pour le transport des cargos du RE au Golgi sur lesquelles se forment les vésicules COPII (The ER exit sites are specialized ER zones for the transport of cargo proteins from the ER to the Golgi apparatus 2019).
2. Malgré l'importance de COPII, l'EGT peut se produire même en l'absence de COPII (une revue dans ER–Golgi transport could occur in the absence of COPII vesicles 2014 et Models of Intracellular Transport: Pros and Cons 2019).
À l'heure actuelle, aucune étude n'a montré que :
- les bourgeons membranaires sur le RE granulaire et vraisemblablement enrobés, contiennent du Sec13 dans leur enveloppe,
- la manière dont les vésicules COPII ou les agrégats de vésicules COPII se déplacent vers le Golgi.
3. Toutefois, le principal problème du VM concerne la sortie des mégacargos, comme d'ailleurs dans l'IGT (
- les préchylomicrons dans les entérocytes,
- les VLDL (lipoprotéines de très basse densité) dans les hépatocytes,
- les agrégats de procollagène,
- des virus relativement gros, dont les virions sont formés dans l'enveloppe nucléaire ou à l'intérieur du RE et ont un diamètre allant jusqu'à 200 nm, comme le virus de l'herpès (Endoplasmic reticulum-to-Golgi transitions upon herpes virus infection 2017).
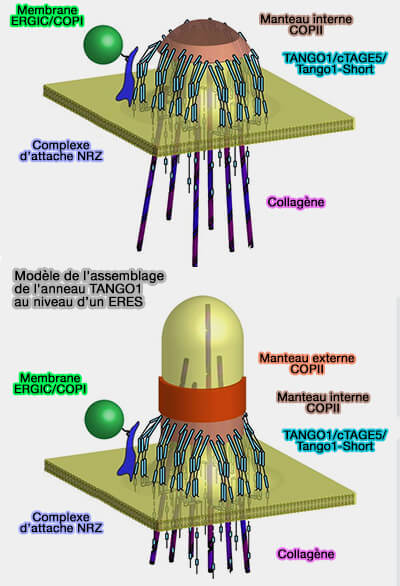
(Figure : vetopsy.fr d'après Raote et coll)
Les mégacargos ne peuvent ni être insérés dans des vésicules COPII de 65 à 80 nm, ni désassemblés en sous-unités plus petites pouvant être emballées dans des vésicules de transport conventionnelles.

Pour étudier finement les contradictions du modèle VM de l'EGT, lire la revue dans Models of Intracellular Transport: Pros and Cons (2019).
Pour résoudre ces contradictions, il a été proposé que les mégacargos soient transportées par des mégavésicules ou des mégatransporteurs formés par des combinaisons inhabituelles d'isoformes de sous-unités COPII.
- Si des mégavésicules existent, Sec13 devrait former un capuchon sur l'agrégat de procollagène, VLDL ou chylomicron.
- La formation des mégabourgeons constitués d'un anneau de l'anneau COPII et d'un anneau plus externe de TANGO1 et montrant des taches positives au procollagène à l'intérieur de ces anneaux n'a pas été démontrée (malgré TANGO1 builds a machine for collagen export by recruiting and spatially organizing COPII, tethers and membranes 2018 et Auto-regulation of Secretory Flux by Sensing and Responding to the Folded Cargo Protein Load in the Endoplasmic Reticulum 2019).
- La démonstration de l'existence des mégavésicules n'est pas convaincante, malgré COPII-coated membranes function as transport carriers of intracellular procollagen I (2017).
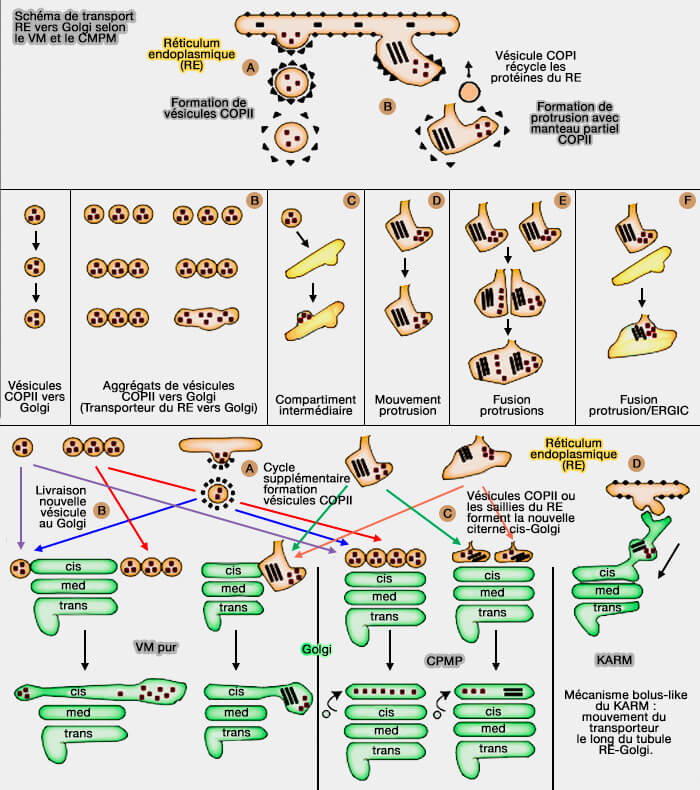
(Figure : vetopsy.fr d'après Mironov et Beznoussenko)

Ainsi, à l'état d'équilibre, les mégabourgeons contenant du procollagène et recouverts d'un revêtement de type COPII n'ont pas été détectés, même ceux de ER-to-Golgi trafficking of procollagen in the absence of large carriers (2019) ou dans les films de Noncanonical autophagy at ER exit sites regulates procollagen turnover (2018).
Modèle de maturation-progression des citernes (CMPM) de l'EGT
1. Le modèle de maturation-progression des citernes (CMPM) suppose que les transporteurs immatures réticulum endoplasmique (RE) vers Golgi sont formés par la protrusion du RE.
Les protéines résidentes du RE sont éliminées des transporteurs RE par des vésicules rétrogrades dépendantes du COPI (ER-to-Golgi Carriers Arise through Direct En Bloc Protrusion and Multistage Maturation of Specialized ER Exit Domains 2003).
2. Le principal argument en faveur du CMPM de l'EGT est décrit dans The ER to Golgi Interface is the Major Concentration Site of Secretory Proteins in the Exocrine Pancreatic (2001).
Une agrégation significativement plus élevée (57,6 fois) du chymotrypsinogène a été observée et le modèle de " concentration par exclusion " a été proposé.
3. Toutefois, les vésicules COPI, qui fonctionnent vraisemblablement comme transporteurs pour le transport rétrograde au niveau de l'ERES (ER Exit Sites), ne peuvent pas être utilisées.
- Ces vésicules COPI ont un rapport très élevé entre leur surface et leur volume, ce qui signifie que ces vésicules ne conviennent pas pour expliquer des niveaux aussi élevés de concentration de cargos.
- Le recyclage des vésicules COPI éliminerait principalement la surface, mais pas le volume des porteurs immatures RE vers Golgi.
- Si les vésicules recouvertes de COPI médient le transport rétrograde, Golgi-à-ER, la concentration de protéines avec des motifs KKxx serait attendue, comme ERGIC53/58 ou p24, dans les bourgeons recouverts de COPI. Cependant, à ce jour, il n'y a eu aucune preuve convaincante démontrant la concentration d'ERGIC53/58 ou de p24 dans les bourgeons recouverts de COPI sur l'ERES.
Pour expliquer de nombreuses observations (revue dans Models of Intracellular Transport: Pros and Cons 2019), deux voies de transport Golgi-RE ont été proposées (Evidence for a COP-I-independent transport route from the Golgi complex to the endoplasmic reticulum 1999) :
- une COPI-dépendante,
- une COPI-indépendante.
(Figure : vetopsy.fr d'après Mironov et coll)
La concentration des protéines résidentes du RE et de l'ERES dans les vésicules COPI dérivées des transporteurs Golgi vers RE devrait être plus élevée que dans les transporteurs RE vers Golgi pour infirmer ou confirmer la CMPM de l'EGT.
Modèle de diffusion (DM)
de l'EGT
1. Dans le cadre du modèle de diffusion (DM), l'EGT se produit par diffusion le long de liaisons constantes entre le réticulum endoplasmique (RE) et l'appareil de Golgi.
Malgré de nombreuses études (revue dans Models of Intracellular Transport: Pros and Cons 2019), personne n'a confirmé la possibilité que le réservoir RE puisse être inséré dans un empilement de saccules du Golgi comme il a été décrit dans Golgi Structure in Three Dimensions: Functional Insights from the Normal Rat Kidney Cell (1999).
2. Les caractéristiques précises du DM d'EGT ne sont pas encore précisées.
Modèle KARM de l'EGT
(Kiss-And-Run Model)
Le modèle KARM (Kiss-And-Run Model), en particulier le modèle asymétrique de l'EGT, présuppose que la fusion entre deux compartiments consécutifs se produit avant la fission, qui a lieu dans la zone où des tubules minces (ou des amincissements du compartiment proximal) doivent être présents.
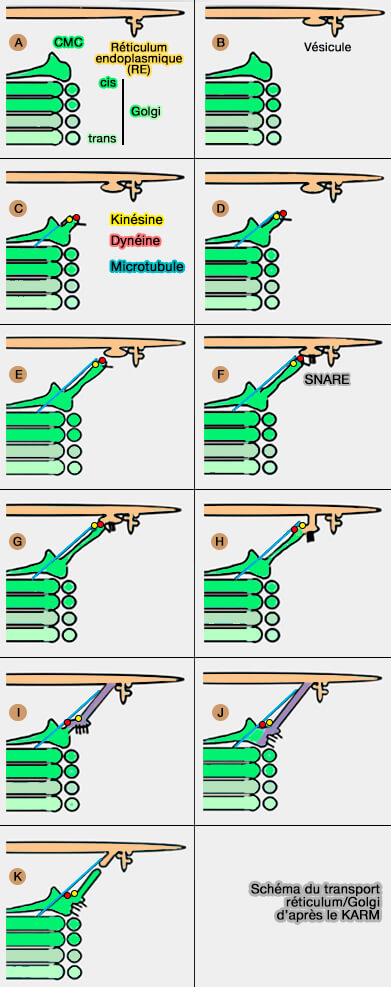
1. Dans un premier temps, la protrusion membranaire contenant un cargo se forme, i.e. petits (A) ou mégacargos (B) dans l'ERES.
2. Un tubule émane de l'appareil de Golgi, et en particulier du CMC (Cis-Most Cisterna) la citerne la plus cis du Golgi (C).
3. Comme la distance entre les compartiments proximaux et distaux est grande, le compartiment distal est étendu vers le proximal, i.e. le tubule qui émane du CMC se dirige vers l'ERES et atteint cette cible en se déplaçant le long d'un microtubule (D-F).
- Ce tubule pourrait utiliser la kinésine, moteur des microtubules, pour son mouvement le long du microtubule.
- La kinésine est présente sur les membranes qui circulent entre le RE et le Golgi, et sa présence sur les structures ERGIC est difficile à concilier avec la VM, car le transport vers le Golgi est dirigé vers l'extrémité négative.
4. Ce microtubule fusionne avec l'ERES (G-H) à l'aide de protéines SNARE et délivre de la dynéine au transporteur RE vers le Golgi, capturant ainsi le cargo (Maturation-driven transport and AP-1–dependent recycling of a secretory cargo in the Golgi 2019).
L'arrivée de ce transporteur génère un flux de Ca++ à partir de l'ERES (ER Exit Sites) et stimule la fusion du transporteur avec le Golgi (The SPCA1 Ca2+ Pump and Intracellular Membrane Trafficking 2010).
5. Le bolus se déplace vers l'appareil de Golgi en utilisant la dynéine et les microtubules. Le transporteur RE vers Golgi se retrouve alors dans la citerne la plus cis ((I,J).
6. Enfin, la fission se produit près du col qui relie la protrusion au RE (K)
Remarque : Tango1 pourraie former des canaux pour le procollagène qui relient le RE au Golgi (Protein transport by vesicles and tunnels 2019 et TANGO1 builds a machine for collagen export by recruiting and spatially organizing COPII, tethers and membranes 2018).
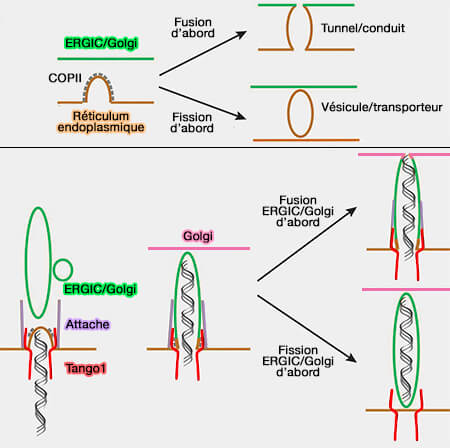
(Figure : vetopsy.fr d'après Raote et Malhotra)
a. La cargaison, le moment de la fission et l'organisation spatiale des compartiments dictent la nature des intermédiaires de transport.
- Les vésicules bourgeonnantes peuvent fusionner avec la membrane cible, créant un tunnel entre le donneur et l'accepteur.
- Si la fission précède la fusion, cela générera une vésicule autonome.
b. Le recrutement d'un compartiment en aval vers le site de bourgeonnement crée la voie de sortie via un tunnel.
- Pour les mégacargos telles que les procollagènes et les lipoprotéines, les protéines de la famille TANGO1 capturent le cargo et les membranes post-RE.
- Les membranes attachées fusionnent les unes avec les autres et avec le bourgeon naissant au RE. Dans ce cas, l'intermédiaire de transport est en fait le compartiment aval de la voie de sécrétion.
- La membrane attachée dans les cellules de mammifères serait l'ERGIC. À ce stade, une nouvelle fusion de l'ERGIC au Golgi pourrait même aboutir à un long tube RE-ERGIC-Golgi.

Ainsi, le VM, le DM et le CMPM ne peuvent pas expliquer toutes les données, alors que le KARM pourrait expliquer les observations fondamentales du VM, du DM et du CMPM.
Retour au système endomembranaire
Biologie cellulaire et moléculaireConstituants de la celluleTransport membranaireTransports sans mouvements membranairesTransports passifsTransports actifsTransports avec mouvements membranaires : trafic vésiculaireFusion/fission membranaireEndocytoseVoie sécrétoireCanaux ioniquesTransporteursUniportsPompesCo-transporteursMoteurs moléculairesVoies de signalisation


