Neurophysiologie phéromonale
Organe voméronasal
Récepteurs : vue d'ensemble, V1R et FRP
- Sens chimiques
- Olfaction
- Vue d'ensemble du système olfactif accessoire (VNS) et des phéromones
- Généralités sur les phéromones
- Perception des phéromones
- Neurophysiologie phéromonale
- Sécrétions
et excrétions contenant des phéromones
- Régions
cutanées sécrétrices des phéromones
- Glandes anales
- Glandes jugales
- Glandes podales
- Sécrétions maternelles
- Sécrétions ou excrétions non cutanées
contenant des phéromones
- Phéromones urinaires
- Autres excrétions
- Régions
cutanées sécrétrices des phéromones
- Phéromones et communication
- Phéromonothérapie
- Gustation
- Vision
- Système somatosensoriel

Les récepteurs de l'organe voméronasal sont constitués principalement par les récepteurs voméronasaux, V1R et V2R.
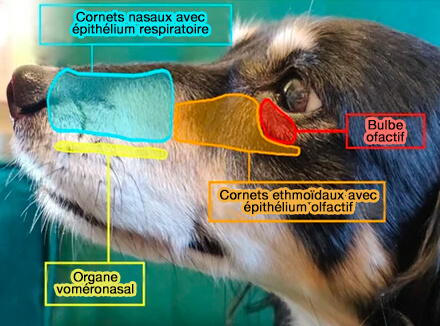
(Photo : vetopsy.fr d'après Buzek et coll)
Signaux olfactifs de reconnaissance
Au niveau des récepteurs cellulaires, les stimuli volatils (odeurs) se lient à des ensembles distincts de récepteurs olfactifs dans l'épithélium olfactif (MOE) tandis que les signaux phéromonaux sont activement pompés dans l'organe voméronasal (VNO) et activent les neurones voméronasaux (VSN) (
1. Chez l'émetteur des signaux sémiochimiques, un nombre croissant de familles de gènes ont été impliquées soit dans le codage des signaux olfactifs, soit dans la présentation ou la stabilisation des signaux.
2. Chez le récepteur, il existe plusieurs familles de gènes qui codent pour les récepteurs qui détectent les signaux sémiochimiques et structurent les circuits neuronaux qui transmettent les signaux au cerveau (From Pheromones to Behavior 2009).
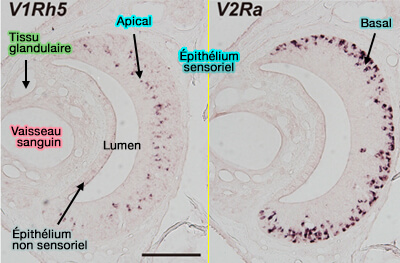
a. On trouve deux grands types de récepteurs voméronasaux qui se répartissent en deux couches :
- une apicale avec les récepteurs V1R,
on trouve aussi ainsi que des récepteurs FPR chez la souris.
- une basale avec les récepteurs V2R, qui ne sont pas présents chez un nombre important d'espèces dont le chien et le chat.
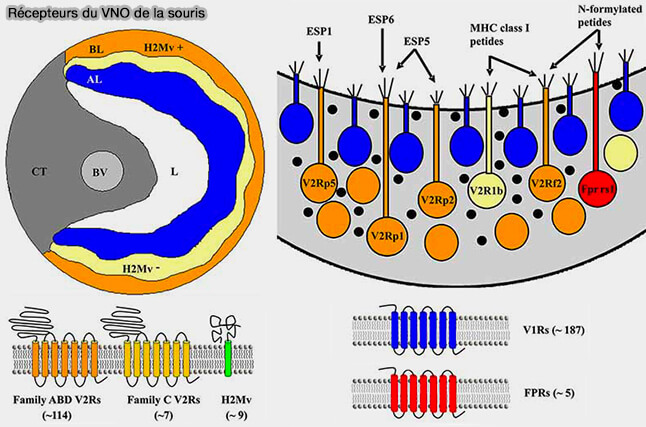
(Figure : vetopsy.fr d'après Pérez-Goméz et coll)
b. On trouve aussi des récepteurs de l'épithélium olfactif (MOE) :
- des récepteurs olfactifs (OR) qui se retrouvent dans le VNO,
- des récepteurs TAAR (Trace amine-associated receptor) qui semblent intervenir dans la reconnaissance des sexes et le statut social d'un individu,
- des récepteurs des glomérules à " collier ", i.e. récepteurs GC-D et MS4A.
c. D'autres gènes individuels codent pour des protéines impliquées dans les processus de transduction du signal spécifiques au VNO qui influencent une gamme de comportements.
3. Ces récepteurs appartiennent à la superfamille des récepteurs couplés aux protéines G (GPCR), sauf les MS4A.
- Chaque membre présente une séquence protéique différente, ce qui suggère que chaque famille peut détecter une variété de produits chimiques.
- les récepteurs chimiosensoriels de l'épithélium olfactif (MOE), i.e. environ 1 000 récepteurs odorants (OR) différents et 14 récepteurs associés aux traces d'amines (TAAR)] appartiennent aussi aux GPCR.
Récepteurs voméronasaux
Chez les rongeurs, les cellules sensorielles de l'organe voméronasal (VNO) se répartissent en deux couches, apicale et basale qui diffèrent selon (Comparative genomic analysis identifies an evolutionary shift of vomeronasal receptor gene repertoires in the vertebrate transition from water to land 2007) :
- l'expression de la famille de protéine G,
- les cibles de projection vers le bulbe olfactif accessoire (AOB).
Toutefois, cette distinction spatiale entre les neurones apicaux et basaux n'est en aucun cas absolue, mais nous utiliserons ces termes par la suite.
| Récepteurs olfactifs (sens large) |
Homme | Souris | Rat | Chien | Vache | Poulet | Grenouille | Poisson zèbre |
|---|---|---|---|---|---|---|---|---|
| Récepteurs phéromonaux | ||||||||
| V1R | 5 (115) |
187 (121) |
106 (66) |
8 (33) |
40 (45) |
0 (0) |
21 (2) |
2 (0) |
| V2R | 0 (7) |
70 (139) |
59 (109) |
0 (5) |
0 (8) |
0 (0) |
249 (448 |
44 (8) |
| Récepteurs olfactifs | ||||||||
| OR | 388 (414) |
1037 (354) |
1201 (292) |
876 (326) |
970 (1159) |
82 (476) |
410 (418) |
102 (35) |
| TAAR | 6 (3) |
15 (1) |
17 (2) |
2 (2) |
17 (9) |
3 (0) |
2 (1) |
109 (110) |
Remarque : le tableau ci-dessus qui date de 2009 permet d'avoir une idée approximative du nombre de gènes intacts, ainsi qu'entre parenthèses, le nombre de pseudogènes, i.e. gènes inactifs au sein d'un génome, du fait d'altérations génétiques les rendant non fonctionnesl et donc incapables de conduire à l'expression d'une protéine (From Pheromones to Behavior 2009).

Le nombre de récepteurs olfactifs a bien augmenté depuis.
Neurones apicaux
Les neurones apicaux expriment :
- la famille des récepteurs du récepteur voméronasal 1 (V1R),
- la plupart des membres de la famille des récepteurs formyl-peptide (FPR).
Les neurones apicaux projettent leurs axones sur la moitié antérieure du bulbe olfactif accessoire (aAOB).
Récepteurs V1R
Nombre et évolution des V1R
Les V1R ont été particulièrement bien étudiés chez la souris, appelés Vmn1r et sont représentés par 12 clades de a à l comptent environ 392 membres à l'heure actuelle, dont 153 pseudogènes (Extreme variability among mammalian V1R gene families 2010).
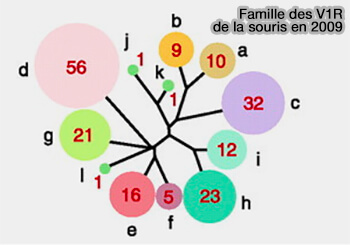
(Figure : vetopsy.fr d'après Tirindelli et coll)
1. L'expression monoallélique du gène Vmn1r garantit que chaque neurone voméronasal (VSN) affiche un seul type de récepteur V1R obtenant ainsi une identité fonctionnelle distincte, i.e. un neurone, un récepteur.
2. Le nombre de V1R varie avec les espèces (The genomic basis of vomeronasal-mediated behaviour 2014).
a. Les analyses évolutives des V1R révèlent que des séquences de récepteurs étaient présentes chez l'ancêtre commun des mammifères placentaires et marsupiaux (Divergent V1R repertoires in five species: Amplification in rodents, decimation in primates, and a surprisingly small repertoire in dogs 2005).
- On trouve des extensions et des suppressions spécifiques à certaines espèces de certaines sous-familles, même dans des lignées aussi proches que celles de la souris et du rat.
- Les pseudogènes trouvés chez les chiens et les primates appartiennent à tous les principaux clades de l'arbre phylogénétique V1R, ce qui indique que l'ancêtre commun possédait un répertoire de récepteurs diversifié qui a ensuite été perdu et dégénéré chez ces espèces, tout en étant maintenu et étendu chez les animaux ayant un rsystème voméronasal développé.
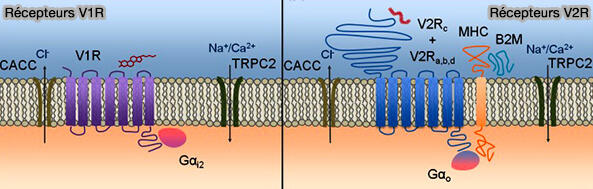
(Figure : vetopsy.fr d'après Ibarra-Soria et coll)
b. Par conséquent, le répertoire V1R des mammifères a probablement été façonné par la niche écologique de chaque espèce comme dans les deux exmples suivants (More Functional V1R Genes Occur in Nest-Living and Nocturnal Terricolous Mammal 2010).
- Les espèces qui vivent dans des nids, i.e. utilité de la vision et de l’ouïe limitée, possèdent des répertoires plus vastes que celles vivant dans des zones ouvertes.
- Les animaux nocturnes possèdent une plus grande collection de V1R que les espèces diurnes.
3. Une corrélation positive a été observée entre le nombre de V1R, la complexité du système voméronasal et la taille du bulbe olfactif accessoire (AOB).
Mécanisme et rôles
1. Les récepteurs V1, V1R, liés à la protéine G Gai2 sont situés dans le compartiment apical du VNO (Evolution of V1R pheromone receptor genes in vertebrates: diversity and commonality 2019).
Comme les récepteurs olfactifs (OR), les TAAR et les récepteurs du goût amer T2R, les V1R et les récepteurs du formyl peptide (FPR) sont des récepteurs couplés aux protéines G (GPCR) de classe A, de type rhodopsine.
(Figure : vetopsy.fr d'après Nikaido)
2. Les V1R réagissent avec une grande sensibilité aux molécules organiques de faible poids moléculaire, en particulier par des composants volatils urinaires.
a. Les stéroïdes sulfatés, qui sont présents dans l'urine des femelles, seraient responsables de l'essentiel de la bioactivité (Sulfated Steroids as Natural Ligands of Mouse Pheromone-Sensing Neurons 2008).
- Ils activent aussi bien les neurones voméronasaux (VSN) des mâles et des femelles.
- Certains récepteurs répondent à des stéroïdes spécifiques, d'autres reconnaissent plusieurs composés chimiquement apparentés (Molecular Organization of Vomeronasal Chemoreception 2011).
b. la suppresion de certains gènes, en particulier les Vmn1r provoquent des modifications comportementales (Deficient pheromone responses in mice lacking a cluster of vomeronasal receptor genes 2002).
Récepteurs FPR
Les neurones apicaux expriment aussi la plupart des membres de la famille des récepteurs formyl-peptide (FPR) qui projettent aussi sur la moitié antérieure du bulbe olfactif accessoire ou aAOB (Formyl peptide receptors are candidate chemosensory receptors in the vomeronasal organ 2009 et Formyl peptide receptor-like proteins are a novel family of vomeronasal chemosensors 2009).
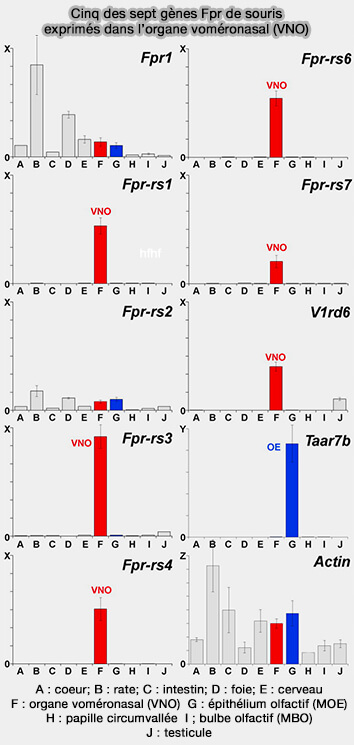
(Figure : vetopsy.fr d'après Liberles et coll)
1. Chez la souris, leur nombre est faible, 5 seulement, i.e. Fpr-rs1, Fpr-rs3-4-6-7 et semble résulter de duplications génétiques récentes et d'une sélection positive (Formyl Peptide Receptors from Immune and Vomeronasal System Exhibit Distinct Agonist Properties 2012).
- Les FPR pourraient reconnaître des ligands sensoriels qui ne sont détectés ni par les V1R ni par les V2R, car ils ne présentent aucune similarité de séquence avec les V1R ou les V2R, mais aussi avec les récepteurs olfactifs (OR) ou aux TAAR exprimés dans l'épithélium olfactif (MOE).
- Alternativement, les FPR pourraient reconnaître certains des mêmes ligands que les V1R ou les V2R, mais générer des signaux transmis à différentes régions du cerveau, permettant ainsi des réponses différentes aux mêmes ligands.
2. Fpr-rs1 est coexprimé avec Gαo, comme V2R, mais les quatre autres sont coexprimés avec Gαi2, comme V1R, ce qui laisse penser que les entrées sensorielles de différents VNO FPR pourraient finalement être ciblées sur différentes zones cérébrales ayant des fonctions distinctes.
3. Leur rôle n'est pas encore bien précisé (The Formyl Peptide Receptors: Diversity of Ligands and Mechanism for Recognition 2017).
a. La famille des FPR offre une protection contre les maladies immunologiques.
Les FRP du système immunitaire Fpr1 et Fpr2 chez la souris, ou FRP1-3 chez l'homme sont retrouvés dans les neutrophiles, les monocytes et autres leucocytes phagocytaires du système immunitaire inné (The Role of Formyl Peptide Receptors in Neurological Diseases via Regulating Inflammation 2021).
FPR1 et FPR2, non localisés dans les VSN, fonctionnent comme des capteurs pour divers attracteurs chimiques qui guident les cellules immunitaires phagocytaires vers les sites d'invasion et d'inflammation d'agents pathogènes.
FPR3, i.e. FPR-rs1, se trouve à la fois dans les cellules immunitaires et dans les VSN, ce qui suggère qu'il pourrait jouer un rôle distinct dans chaque système (Strain-specific Loss of Formyl Peptide Receptor 3 in the Murine Vomeronasal and Immune Systems 2016).
- b. Les gènes Fpr-rs3, 4, 6 et 7 se trouvent sélectivement dans les neurones VNO et peuvent ainsi être désignés comme FPR voméronasaux et détectent des signaux associés à l'état pathogène d'un individu tels que les peptides formylés (The Vomeronasal System Mediates Sick Conspecific Avoidance 2015) et d'autres ligands liés à l'inflammation (Recognition of Bacterial Signal Peptides by Mammalian Formyl Peptide Receptors 2015).
Chez les rongeurs, leur présence dans le VNO provoquerait des comportements d'évitement pour résister à l'infection, rôle perdu dans les autres espèces.
Neurones basaux : récepteurs V2R
Sens chimiquesOlfactionCommunication olfactiveVue d'ensemble du système olfactif accessoire (VNS) et des phéromonesPerception phéromonaleOrgane voméronasal (VNO)Transduction voméronasaleBulbe olfactif accessoire (AOB)Voies ascendantesSécrétions et excrétions phéromonalesCommunication phéromonalePhéromones et marquagesPhéromones et organisation socialePhéromones et reproductionPhéromones et alarmePhéromonothérapie


