Transport membranaire
Transports sans mouvements membranaires
Transporteurs actifs : co-transporteurs (transporteurs secondaires)
Modèle rocker-switch (interrupteur à bascule) : modèle symétrique
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Le modèle rocker-switch (" commutateur ou interrupteur à bascule "), le plus simple, est l'un des trois mécanismes des co-transporteurs.
1. La plupart des co-transporteurs peuvent être décrits comme fonctionnant sous :
- le modèle rocker-switch (" commutateur ou interrupteur à bascule "), le plus simple,
- le modèle rocking-bundle (" faisceau à bascule ").
2. Le modèle elevator (" ascenseur ou élévateur ") a été envisagé plus récemment.
Mécanisme symétrique simple : transporteurs SemiSWEET
1. Le mécanisme le plus simple de rocker-switch correspond à des mouvements rigides de deux faisceaux, liés de manière symétrique autour d'un site de liaison de substrat situé au centre (Structural advances for the major facilitator superfamily (MFS) transporters 2013 et Substrate-induced changes in the structural properties of LacY 2014).

La protéine se déplace autour du substrat, exposant alternativement le site de liaison de chaque côté de la membrane.
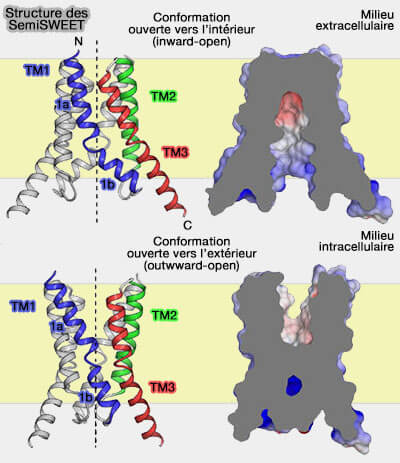
(Figure : vetopsy.fr d'après Yongchang lee et coll)
2. Les transporteurs SWEET sont des transporteurs de sucre chez les plantes et les animaux.
a. Les homologues bactériens des transporteurs SWEET de sucre, les SemiSWEET, ont un fonctionnement le plus simple et le plus proche d'un mécanisme d'interrupteur à bascule (Crystal structure of a bacterial homologue of SWEET transporters 2015 et Structures of SemiSWEET transporters in two distinct conformations 2015).
Les SWEET, ou famille à PQ-loop, font partie de la superfamille TOG (Transporter-Opsin-G protein-coupled receptor Superfamily 2013).
b. Les SemiSWEET se présentent sous forme de dimères dont l'axe central est perpendiculaire à la membrane et dont les extrémités N-terminales sont extracellulaires et les extrémités C-terminales intracytoplasmiques (topologie Nout-Cin).

Ce chapitre est largement inspiré de l'article : Structural basis for the facilitative diffusion mechanism by SemiSWEET transporter (2015).
Structure globale
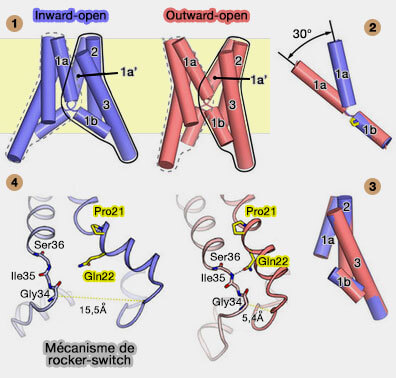
(Figure : vetopsy.fr d'après Yongchang lee et coll)
Chaque protomère comprend trois hélices transmembranaires, TM1, TM2 et TM3.
- TM1 est plié à Pro21 dans le motif PQ-loop hautement conservé qui sépare cette hélice en deux parties (TM1a et TM1b).
- L'hélice courte TM2 est presque entièrement enfouie à l'intérieur de la membrane.
- La longue hélice TM3 fait saillie dans l'environnement aqueux du côté intracellulaire.
Les six hélices TM des deux protomères créent une cavité centrale d'une dizaine d'Å le long de l'axe central, adaptée pour accueillir un saccharide ou un disaccharide au milieu du noyau dimérique.
- Dans la conformation ouverte vers l'intérieur (IF : inward-facing ou inward-open), cette cavité est complètement occluse du côté extracellulaire et de l'environnement lipidique par l'association étroite des régions extracellulaires des hélices TM.
- Dans la conformation ouverte vers l'extérieur (OF : outward-facing ou outward-open), cette cavité est complètement fermée du côté intracellulaire par le rapprochement des hélices TM intracellulaires alors que les parties extracellulaires des protomères sont séparées les unes des autres.
Configurations
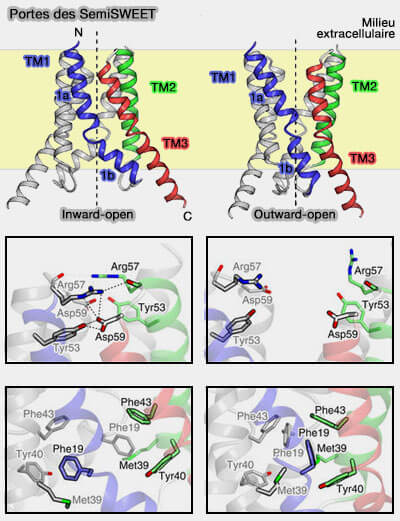
(Figure : vetopsy.fr d'après Yongchang lee et coll)
Boucle PQ (PQ-loop)
La comparaison structurale des protomères dans les conformations ouvertes vers l'intérieur et vers l'extérieur a révélé plusieurs différences :
- un coude d'environ 30° entre TM1a et TM1b s'est formé à Pro21 dans le motif de boucle PQ,
- un mouvement de rotation relatif des deux faisceaux d'hélice symétriques, constitués de TM1b, TM2 et TM3 d'un protomère et TM1a de l'autre protomère (entourés sur la figure ci-contre).
Chaque faisceau d'hélice des deux conformations peut être bien superposé, ce qui suggère un mouvement rigide du corps de la protéine (c).
- En outre, Gln22 (Q22) dans le motif PQ-boucle interagit avec les atomes de la chaîne principale des résidus sur la boucle intracellulaire reliant TM1 et TM2.
- Gln22 peut stabiliser la charnière en pontant les deux faisceaux d'hélice pour permettre un changement structurel dynamique dans TM1b et la boucle cytoplasmique suivante.
Cette boucle PQ sert de charnière flexible, permettant ainsi le mouvement de " binder clip-like " (en français, pince-notes ou pince double clip), dans lequel l'ouverture de la cavité extracellulaire est couplée à la fermeture de la cavité intracellulaire.
Portes extra- et intracellulaires
Les structures des conformations ouvertes vers l'intérieur et vers l'extérieur ont révélé la présence de deux portes distinctes sur les côtés extracellulaire et intracellulaire, qui limitent l'accessibilité de la poche de liaison au substrat.
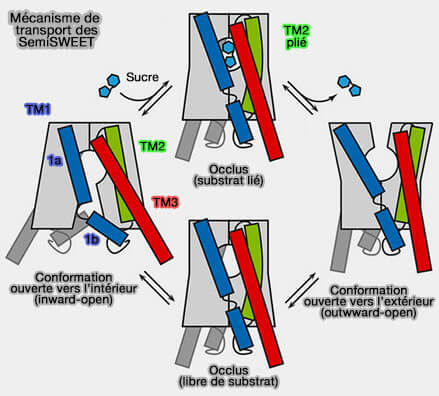
(Figure : vetopsy.fr d'après Yongchang lee et coll)
1. La porte extracellulaire est formée par les résidus d'acides aminés sur une boucle reliant TM2 et TM3.
- Dans la conformation ouverte vers l'intérieur, Tyr53, Arg57 et Asp59 interagissent avec les résidus équivalents du protomère adjacent : ces interactions obturent complètement la poche de liaison au substrat de l'environnement extracellulaire.
- Dans la conformation ouverte vers l'extérieur, en raison des mouvements qui éloignent les TM2/TM3 de chaque protomère, ces liaisons sont brisées.
2. La porte intracellulaire est formée par des résidus hydrophobes sur TM1 et TM2.
- Dans la conformation ouverte vers l'intérieur, Phe19, Met39, Tyr40 et Phe43 des deux protomères, résidus aromatiques et hydrophobes, interagissent pour fermer la porte interne.
- Dans la conformation ouverte vers l'extérieur, ces résidus hydrophobes sont séparés les uns des autres, créant ainsi une cavité cytoplasmique qui permet l'accès du substrat à la poche de liaison au substrat.
(Video : Yongchang lee et coll)
3. Une autre étude décrit une conformation occluse des deux côtés (Structures of SemiSWEET transporters in two distinct conformations 2015).
- Les deux portes, extracellulaire et intracellulaire, sont fermées chez L. biflexa SemiSWEET (LbSemiSWEET), dans lequel les résidus décrits précédemment sont complètement conservés.
- Une comparaison structurale des deux conformations distinctes de l'EcSemiSWEET et de la conformation occluse de LbSemiSWEET a révélé une légère courbure à TM2 dans le LbSemiSWEET. Ce coude permet la fermeture des deux portes dans la conformation occluse.

Dans ces transporteurs primitifs, les faisceaux d'hélices constituant chaque pièce du mécanisme ne bougent pas en tant que corps rigide strict, mais peuvent légèrement se plier.
Comme le résidu proline est hautement conservé dans les SWEET et les transporteurs de la famille PQ-loop, ce mouvement pourrait être conservé chez tous ces transporteurs.
Mécanismes asymétriques
Biologie cellulaire et moléculaireConstituants de la celluleMatrice extracellulaireReproduction cellulaireTransport membranaireCanaux ioniquesTransporteursUniportsPompesCo-transporteursMécanismes des transporteursRocker-switchRocking-bundleElevatorTrafic vésiculaireMoteurs moléculairesVoies de signalisation


